SARM1 Inhibitors Market GRÖSSEN- UND MARKTANTEILSANALYSE - WACHSTUMSTRENDS UND PROGNOSEN (2024 - 2031)
SARM1 Inhibitors Market wird durch Indikation (Amyotrophe Lateralsklerose, Multiple Sklerose, Peripheral Neuropathien, Glaucoma) segmentiert Nach Art ....
SARM1 Inhibitors Market Größe
Marktgröße in USD Mn
CAGR103.7%
| Studienzeitraum | 2024 - 2031 |
| Basisjahr der Schätzung | 2023 |
| CAGR | 103.7% |
| Marktkonzentration | Medium |
| Wichtige Akteure | Abwehrtherapie, Nura Bio, Washington University, Asha Therapeutics, UZB Pharma und unter anderem |
Bitte lassen Sie es uns wissen!
SARM1 Inhibitors Market Analyse
Die SARM1 Inhibitoren Der Markt wird geschätzt USD 5 Mio. in 2024 und wird voraussichtlich erreichen USD 727 Mn von 2031Wachstumsrate (CAGR) von 103,7% von 2024 bis 2031.
Der Markt wird voraussichtlich über den Prognosezeitraum ein positives Wachstum verzeichnen. Faktoren wie hohe Prävalenz neurologischer Störungen wie Rückenmarksverletzungen und wachsende Forschung und Entwicklung für neue Arzneimittelmoleküle werden erwartet, die Nachfrage zu treiben. Die Vermehrung der klinischen Testergebnisse von SARM1-Inhibitoren bei der Behandlung verschiedener neurologischer Bedingungen wird weitere Impulse für das Wachstum geben. Zusätzlich wird erwartet, dass die steigende geriatrische Bevölkerung anfällig für neurologische Krankheiten, die mit steigenden Gesundheitsausgaben ergänzt werden, die Einkommensentwicklung unterstützt.
SARM1 Inhibitors Market Trends
Markttreiber - Erhöhung der Investitionen in die neurologische Forschung, insbesondere in SARM1-Hemmung, treibt den Markt voran
Die Investitionen in die neurologische Forschung sind in den letzten Jahren stetig gestiegen. Es gab eine wachsende Anerkennung der Auswirkungen neurodegenerativer Erkrankungen auf die öffentliche Gesundheit und Wirtschaft. Mehrere Förderagenturen und Stiftungen haben ihre Budgets erhöht, um Behandlungen für Bedingungen wie Alzheimer, Parkinson und ALS zu finden. Die Erforschung der Mechanismen der Axon-Degeneration hat erhebliche Unterstützung erhalten. Ein vielversprechender neuer Bereich ist die SARM1-Hemmung.
Studien haben festgestellt, dass SARM1 spielt eine Schlüsselrolle in der Axon Selbstzerstörung, vor allem nach Verletzung. Die Blockierung von SARM1 könnte Nervenschäden durch verschiedene neurologische Beleidigungen und Krankheiten verhindern. Dies hat großes Interesse sowohl von öffentlichen als auch von privaten Geldgebern geweckt. In den letzten fünf Jahren haben sich die NIH-Zuschüsse auf die SARM1-Biologie konzentriert und ihr therapeutisches Potenzial verdoppelt. Mehrere Pharma- und Biotech-Unternehmen haben auch diesen Bereich durch Akquisitionen und interne Forschungsinitiativen aufgenommen. Einige haben Kandidateninhibitoren in präklinische und klinische Tests vorangebracht.
Markttreiber - Die steigende Prävalenz neurodegenerativer Erkrankungen weltweit
Neurodegenerative Bedingungen wie Alzheimer und Parkinson steigen mit einer alarmierenden Rate, da die Bevölkerung weltweit altert. Es wird geschätzt, dass derzeit über 50 Millionen Menschen mit Demenz leben und die Zahlen in den kommenden Jahrzehnten verdreifacht werden. Selbst in Ländern mit verbesserten Gesundheitssystemen und Lebenserwartung steigt die Prävalenz dieser Krankheiten unabdingbar. Die persönliche und gesellschaftliche Belastung der Neurodegeneration ist enorm und wird weiter wachsen, wenn keine effektiven Behandlungsoptionen zur Verfügung stehen.
Patienten und ihre Pflegepersonen sind verzweifelt nach Therapien, die Krankheitsfortschritte verlangsamen oder stoppen können. Der Mangel an zugelassenen krankheitsmodifizierenden Behandlungen hat einen großen unpassenden Bedarf hinterlassen. Zahlreiche klinische Studien potenzieller Therapien haben in den letzten Jahren aus verschiedenen Gründen gescheitert. Dies hat die Dringlichkeit erhöht, um neue Wege und Ziele zu erkunden. SARM1-Hemmung ist eine vielversprechende Allee, da sie Neuroprotektion in einer breiten Palette von neurologischen Bedingungen bieten könnte. Die Blockierung des SARM1-Wegs kann sich als krankheitsmodifizierend und nicht nur symptomatisch erweisen. Bedeutende Ressourcen werden zur Validierung von SARM1 als Drogenziel für die Neurodegeneration eingesetzt.

Markt Challenge - Die hohen Kosten und Komplexität der Medikamentenentwicklung für neurodegenerative Störungen können Marktwachstum begrenzen
Die Entwicklung von Medikamenten zur Behandlung neurodegenerativer Erkrankungen stellt erhebliche Herausforderungen aufgrund der komplexen Natur der Krankheiten und des begrenzten Verständnisses von Krankheitswegen und Mechanismen dar. Drogenentdeckung und -entwicklung beinhaltet lange klinische Studienzeiten über mehrere Jahre, um Wirksamkeit und Sicherheit zu testen. Neurodegenerative Erkrankungen betreffen jedoch typischerweise ältere Bevölkerungsgruppen, die aufgrund von Komorbiditäten für klinische Studien nicht geeignet sind. Darüber hinaus können Ergebnisse schwierig sein, objektiv zu messen und Endpunkte müssen Veränderungen in der Funktionsweise über viele Jahre zeigen, um Nutzen zu zeigen. Diese Komplexitätsfaktoren tragen zu hohen Entwicklungskosten bei, mit Schätzungen von 800 Millionen Dollar bis 2 Milliarden Dollar für jedes neue Medikament. Die Hersteller müssen die Kostenrückgewinnung berücksichtigen und hohe FuE-Investitionen mit Preisen ausgleichen. Das Risiko des Drogenversagens bleibt auch nach großen Investitionen hoch. Diese Marktbarrieren können Investitionen in seltene Krankheiten wie Neurodegeneration, wo die Zahl der behandelnden Patienten gering ist, disincentivieren. Hohe Drogenpreise könnten auch den Zugang für Patienten begrenzen. Insgesamt stellen die Kosten und die damit verbundenen Unsicherheiten erhebliche Herausforderungen für das Marktwachstum dar.
Marktchance: Fortschritte in der Präzisionsmedizin bieten Wachstumspotenzial
In den letzten Jahren haben große Fortschritte beim Verständnis von genetischen Beiträgen und molekularen Pfaden, die an neurodegenerativen Störungen beteiligt sind, beobachtet. Dies ermöglichte die Anwendung von Präzisions- oder personalisierten Medikamentenansätzen zur gezielten Patientensubpopulation. Beispielsweise ermöglicht die Identifizierung von Biomarkern, die Patienten auf Basis von Krankheitssubtypen oder Progressionsstufen straffen, eine deutlichere Bewertung der Wirksamkeit von Medikamenten. Auch bei der Entwicklung von Therapien, die auf genetische Mutationen im Zusammenhang mit familiären Formen von Krankheiten zugeschnitten sind, werden Fortschritte erzielt. Diese personalisierten Strategien versprechen, Untergruppen von Patienten effektiver zu behandeln. Darüber hinaus bieten aufstrebende Technologien wie Computermodellierung von Gehirnnetzwerken Potenzial, um Drogeneffekte besser vorherzusagen und Dosierregime zu optimieren. Solche Präzisionsansätze sollen Vorteile maximieren und Nebenwirkungen für Patienten minimieren. Wenn erfolgreich, könnten sie höhere Drogenpreise rechtfertigen und weitere Investitionen fördern. Insgesamt bieten laufende Fortschritte bei der Schichtung dieser komplexen Erkrankungen ein erhebliches Wachstumspotenzial für molekular gezielte SARM1-Inhibitortherapien.
Präferenzen der Verschreiber von SARM1 Inhibitors Market
Die Behandlung neurodegenerativer Erkrankungen folgt typischerweise einem schrittweisen Ansatz basierend auf Krankheitsverlauf und Schwere der Symptome. Bei milden Fällen der Alzheimer-Krankheit beginnen Verschreibungen häufig mit Cholinesterase-Inhibitor-Medikamenten wie Donepezil (Aricept). Diese Medikamente arbeiten, um Acetylcholinspiegel im Gehirn zu steigern und kognitive Vorteile zu bieten.
Da Alzheimer auf ein moderates Stadium vorankommt, kann die Kombinationstherapie vorgeschrieben werden, um mehrere Symptome anzusprechen. Ein häufiges Regimen ist Donepezil plus memantine (Namenda), ein N-Methyl D-aspartate Rezeptorantagonist. Diese Wirkstoffkombination zielt darauf ab, Gedächtnis, Denken, Verhalten und tägliche Funktion zu verbessern.
Für fortgeschrittene Alzheimer und schwere Demenz werden nicht-pharmakologische Ansätze wichtig. An dieser Stelle bieten Medikamente wenig kognitiven Nutzen, aber kann helfen, Verhaltensweisen wie Aggression, Angst und Schlaflosigkeit zu verwalten. Antipsychotika wie Quetiapin (Seroquel) werden oft für ihre sedierenden Wirkungen Off-Label verwendet.
Jenseits von Medikamenten betrachten Prescriber auch Faktoren wie Versicherung Deckung, Kosten für Patienten, Pflegeunterstützung und Fähigkeit, an Dosierungsplänen zu halten. Ihre Präferenzen können durch klinische Studiendaten sowie Interaktionen mit pharmazeutischen Vertretern und Meinungsführern beeinflusst werden.
Analyse der Behandlungsoptionen von SARM1 Inhibitors Market
Lungenkrebs wird typischerweise in vier Hauptstufen - I, II, III und IV - eingestuft, abhängig von der Größe und Ausbreitung des primären Tumors und ob es metastasiert zu Lymphknoten oder entfernten Organen. Die Behandlungsoptionen variieren je nach Stadium deutlich.
Für die Stufe I nicht-kleinen Zell-Lungenkrebs (NSCLC) ist die bevorzugte Option in der Regel Chirurgie, um den Tumor zu entfernen. Für die Stufe II ist die Operation wiederum die primäre Wahl und kann mit einer adjuvanten Chemotherapie mit einem platinbasierten Doublet wie Cisplatin/Carboplatin mit Medikamenten wie Pemetrexed, Edelsteincitabin oder Taxane ergänzt werden, um das Risiko von Wiederauftreten zu reduzieren. Stage III NSCLC beinhaltet Lymphknoten-Einbindung, so dass es weniger geeignet für Operation allein. Der Standard der Pflege ist die Neoadjuvant Chemotherapie mit Cisplatin/Carboplatin plus ein Taxan, gefolgt von gleichzeitiger Chemoradiation mit einem platinbasierten Regimen mit Strahlentherapie. Es folgt manchmal eine adjuvante Immuntherapie mit Medikamenten wie Pembrolizumab oder Nivolumab, um das Immunsystem gegen Lungenkrebszellen zu aktivieren.
Für die Stufe IV metastasierende NSCLC bleibt die Platindoublet-Chemotherapie eine erstklassige Option. Die Immuntherapie mit PD-1 Inhibitoren wie Pembrolizumab, Nivolumab oder Atezolizumab ist jedoch aufgrund der höheren Wirksamkeit und reduzierten Nebenwirkungen im Vergleich zur Chemotherapie immer prominenter geworden. Für Patienten mit EGFR oder ALK Mutationen werden gezielte Therapien wie Gefitinib, Erlotinib oder Alectinib bevorzugt.
Wichtige Erfolgsstrategien der Hauptakteure von SARM1 Inhibitors Market
Zusammenarbeit und Partnerschaften waren eine große Gewinnstrategie für Unternehmen in diesem Bereich. Im Jahr 2021 trat Cleave Therapeutics eine Zusammenarbeit mit Eli Lilly ein, um SARM1-Inhibitoren für degenerative Erkrankungen zu entwickeln und zu vermarkten. Dies gab Cleave Zugang zu Lillys bedeutenden FuE- und Kommerzialisierungsfunktionen und reduzierte die Entwicklungskosten.
Auch Targeting Indikationen mit hohem Bedarf und Marktpotenzial haben sich bewährt. Im Jahr 2020 entschied sich Astellas für die Entwicklung seines SARM1-Inhibitors ASP-7037 für Spinal Muscular Atrophy (SMA). SMA stellt eine große Marktchance dar, da es nur zwei zugelassene Therapien gibt. Mit dem Ziel dieser Indikation positionierte sich Astellas, einen großen Teil des SMA-Marktes zu erfassen, wenn ASP-7037 genehmigt wird.
Die Konzentration auf neurodegenerative Erkrankungen hat sich ausgezahlt, da sie große Patientenpopulationen darstellen und die Rückerstattung oft günstig ist. Störungen wie ALS, MS und Rückenmarksverletzung haben wenige zugelassene Behandlungsoptionen, so dass SARM1 Inhibitoren eine schnelle Annahme sehen konnten. Cleave und Astrocyte entwickeln aufgrund dieser Strategie gezielt Therapien für ALS und Rückenmarksverletzungen.
Die rasche Förderung von klinischen Programmen hat auch Unternehmen geholfen, eine Wettbewerbsposition zu etablieren. Cleave initiierte eine Phase-1-Studie von CLV-048 innerhalb von 12 Monaten nach der Gründung und Meldung von Anfangsergebnissen in 18 Monaten, was die Progressionsgeschwindigkeit beweist. Schnelle klinische Fortschritte signalisiert Engagement und De-Risiko-Programme von konkurrierenden Therapien.
Licensing genehmigte Technologien beschleunigte Entwicklungszeiten. Im Jahr 2019 lizenzierte Astellas die Rechte an ASP-7037 von Astrocite, so dass es preklinische Arbeit bereits abgeschlossen auf der Verbindung zu nutzen und in klinische Studien schneller als interne Entdeckung voranzutreiben. Dies erlaubte Astellas, einen frühen Vorteil in der Klinik gegen interne Pipeline-Programme zu etablieren.
Segmentanalyse von SARM1 Inhibitors Market
Anzeigen: Unmet medizinische Bedürfnisse treiben die amyotrophen lateralen Sklerose treibt Marktwachstum
Amyotrophe laterale Sklerose (ALS), auch bekannt als Lou Gehrig's Krankheit, trägt das Subsegment aufgrund erheblicher medizinischer Bedürfnisse den höchsten Anteil von 45,7% am SARM1-Hemmermarkt bei. ALS ist eine tödliche neurodegenerative Erkrankung mit begrenzten Behandlungsoptionen und hohen Mortalitätsraten. Derzeit gibt es keine Heilung für ALS und die einzige FDA zugelassene Droge, Riluzole, bietet bescheidene Vorteile. Dies deutet eindeutig auf einen hohen Bedarf an effektiveren Therapien hin.
Die SARM1-Hemmung entsteht als vielversprechender therapeutischer Ansatz für ALS. Präklinische Studien haben gezeigt, dass SARM1 eine kritische Rolle bei der Neuroentzündung und dem neuronalen Zelltod im Zusammenhang mit ALS spielt. Inhibiting SARM1 kann möglicherweise den Krankheitsverlauf stoppen, indem axonale Degeneration und neuronalen Verlust verhindert werden. Mehrere pharmazeutische Unternehmen entwickeln aktiv kleine Moleküle SARM1 Inhibitoren für ALS mit einigen Kandidaten bereits in klinischen Studien. Wenn nachgewiesen sicher und effektiv, diese Inhibitoren können erhebliche klinische Vorteile für ALS-Patienten und sogar der Standard der Pflege.
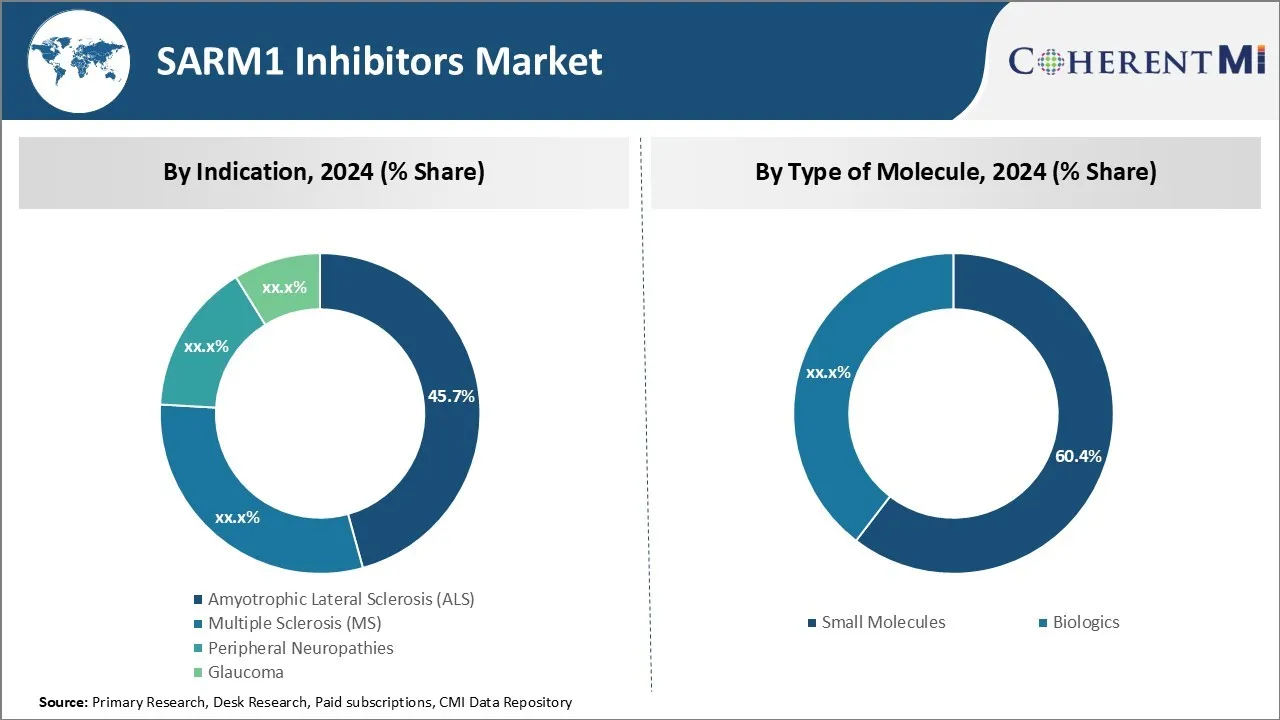
Einblicke, nach Art der Moleküle: Vorteile gegenüber Biologik treiben kleine Moleküle Nachfrage
Das kleine Molekül-Untersegment dominiert den SARM1-Hemmermarkt mit einem Marktanteil von 60,4% aufgrund verschiedener Vorteile gegenüber biologen Molekülen. Kleine Moleküldrogen lassen sich im Vergleich zu Biologen im großen Maßstab leichter entwickeln und herstellen. Sie haben eine bessere Stabilität, erfordern weniger komplexe Lieferkette und Qualitätskontrolle Prüfung. Noch wichtiger ist, dass kleine Moleküle in der Regel eine überlegene Gewebepenetration zeigen und höhere Konzentrationen im zentralen Nervensystem (CNS) erreichen.
Targeting SARM1, ein in Axonen und neuronalen Zellkörpern lokalisiertes Protein, erfordert Inhibitoren mit hervorragender CNS-Pensionsfähigkeit. Die meisten ALS-Patienten haben auch eine signifikante neuromuskuläre Denervation, die Inhibitoren erfordert, die effektiv degenerierende Motorneuronen und neuromuskuläre Verbindungen erreichen können. Kleine Moleküle sind aufgrund ihrer optimalen physikalisch-chemischen Eigenschaften besser ausgerüstet als Biologik, um den Blut-Hirn-Barrier zu überwinden und subzelluläre Standorte der SARM1-Aktion zu erreichen. Diese kritischen pharmakokinetischen Vorteile machen kleine Moleküle SARM1 Inhibitoren sehr wünschenswert für die Entwicklung effektiver ALS Therapien.
Zusätzliche Einblicke von SARM1 Inhibitors Market
- Der Markt für Inhibitoren der SARM1 ist für exponentielles Wachstum gesichert, das durch steigende Investitionen in Forschung, insbesondere in Nordamerika, getrieben wird. Die zunehmende Prävalenz neurodegenerativer Erkrankungen wie ALS und MS, verbunden mit Fortschritten in der Präzisionsmedizin, positioniert SARM1 Inhibitoren als vielversprechende therapeutische Grenze. Die rasche Expansion des Marktes wird auch durch laufende präklinische Studien und die zunehmende Beteiligung von akademischen Institutionen und Biotech-Unternehmen gefördert.
- Die Washington University hat vor allem 64% der Stipendien für die SARM1-Forschung erhalten, was ihre zentrale Rolle bei der Marktinnovation hervorhebt.
Wettbewerbsübersicht von SARM1 Inhibitors Market
Zu den wichtigsten Akteuren im SARM1-Hemmermarkt gehören Disarm Therapeutics, Nura Bio, Washington University, Asha Therapeutics und UCB Pharma.
SARM1 Inhibitors Market Marktführer
- Abwehrtherapie
- Nura Bio
- Washington University
- Asha Therapeutics
- UZB Pharma
SARM1 Inhibitors Market - Wettbewerbsrivalität

SARM1 Inhibitors Market
(Von großen Akteuren dominiert)
(Hoher Wettbewerb mit vielen Akteuren.)
Neueste Entwicklungen in SARM1 Inhibitors Market
- Im April 2024 gab Asha Therapeutics präklinische Studien für ASHA-624 bekannt, eine vielversprechende Therapie, die darauf abzielt, das SARM1-Protein zur Behandlung von ALS zu hemmen, was eine potenzielle Markterweiterung anzeigt.
- Im Juni 2023 sicherte die Washington University die höchsten Stipendien für die SARM1-Forschung und verstärkte ihre führende Position im Markt.
SARM1 Inhibitors Market Segmentierung
- Indikation
- Amyotrophe Lateralsklerose (ALS)
- Multiple Sklerose (MS)
- Periphere Neuropathien
- Glaucoma
- Nach Art der Moleküle
- Kleine Moleküle
- Biologik

Möchten Sie die Möglichkeit erkunden, einzelne Abschnitte dieses Berichts zu kaufen?
Häufig gestellte Fragen :
Was sind die wichtigsten Faktoren, die das Wachstum des SARM1-Hemmermarktes behindern?
Die hohen Kosten und Komplexität der Arzneimittelentwicklung für neurodegenerative Erkrankungen und regulatorische Herausforderungen bei der Zulassung neuer Therapien für neurodegenerative Erkrankungen sind die Hauptfaktoren, die das Wachstum des SARM1-Inhibitorenmarktes behindern.
Was sind die wichtigsten Faktoren, die das Marktwachstum der SARM1-Inhibitoren treiben?
Die zunehmende Investition in die neurologische Forschung, insbesondere in der Sarm1-Hemmung, und die steigende Prävalenz neurodegenerativer Erkrankungen weltweit sind die Hauptfaktoren, die den SARM1-Hemmermarkt antreiben.
Welches ist die führende Indication im SARM1-Hemmermarkt?
Das führende Indikationssegment ist die amyotrophe laterale Sklerose (ALS).
Welche sind die Hauptakteure im SARM1-Hemmermarkt?
Disarm Therapeutics, Nura Bio, Washington University, Asha Therapeutics und UCB Pharma sind die wichtigsten Spieler.
Was wird das CAGR des SARM1-Hemmermarktes sein?
Die CAGR des SARM1-Hemmermarktes wird von 2024-2031 auf 103,7% projiziert.