Cytomegalovirus (CMV) Infecção Mercado Terapêutico ANÁLISE DE TAMANHO E PARTICIPAÇÃO - TENDÊNCIAS DE CRESCIMENTO E PREVISÕES (2024 - 2031)
Cytomegalovirus (CMV) Infection Therapeutic Market é segmentado por tipo de droga (Valgnciclovir, Ganciclovir, Cidofovir, Foscarnet), por aplicação (transplante de grama, transplantação de células estaminais, infecção CMV congênita), por canal de distribuição (Fármacos hospitalares, farmácias de varejo, farmácias on-line), por Geografia (América do Norte, América Latina, Ásia e Pacífico, Ásia, Ásia, Pacífico, O relatório oferece o valor (em USD milhões) para o acima mencionado.
Cytomegalovirus (CMV) Infecção Mercado Terapêutico Tamanho
Tamanho do mercado em USD Mn
CAGR7.10%
| Período de estudo | 2024 - 2031 |
| Ano base da estimativa | 2023 |
| CAGR | 7.10% |
| Concentração de Mercado | Medium |
| Principais jogadores | Moderna, Biociência de Trellis, SpyBiotech, Vários, Bioterapêutica de Atara e entre outros |
por favor, avise-nos!
Cytomegalovirus (CMV) Infecção Mercado Terapêutico Análise
Estima-se que o Global Cytomegalovirus (CMV) Infection Therapeutic Market seja avaliado em USD 231.4 Mn em 2024 e é esperado alcançar USD 370.2 Mn por 2031, crescendo a uma taxa de crescimento anual composta (CAGR) de 7,10% de 2024 a 2031. O mercado tem sido impulsionado principalmente pela crescente incidência de infecções por CMV entre os pacientes de infantes e AIDS, bem como a disponibilidade de drogas de pipeline de última fase que são susceptíveis de entrar no mercado nos próximos anos.
A tendência de mercado mostrou crescimento constante e gradual ao longo dos últimos anos. Pesquisas recentes e parcerias entre empresas têm trabalhado para melhorar técnicas de diagnóstico e desenvolvimento terapêutico para infecção por CMV. Além disso, aumentar a conscientização sobre práticas de higiene e prevenção da infecção tem impactado positivamente o tamanho do mercado. Espera-se que outras inovações para fornecer opções de tratamento mais amplas continuem a conduzir o mercado durante o período de previsão.
Cytomegalovirus (CMV) Infecção Mercado Terapêutico Tendências
Driver de mercado - O número crescente de pacientes imunocomprometidos, como aqueles que recebem transplantes de órgãos ou aqueles que vivem com HIV/AIDS, é a demanda por terapias mais eficazes e vacinas preventivas para CMV.
O número crescente de pacientes imunocomprometidos que são mais suscetíveis à infecção por CMV é um driver chave da demanda por melhores opções de tratamento. Os pacientes que recebem transplantes de órgãos devem tomar medicamentos imunossupressores para prevenir a rejeição do órgão transplantado por seu sistema imunológico. No entanto, isso os deixa vulneráveis a infecções, incluindo CMV. De acordo com estudos, a infecção por CMV é comum após o transplante renal, com 50-80% dos receptores com infecção por CMV no primeiro ano. Para pacientes com transplante de pulmão e coração, a infecção por CMV é uma ameaça grave, com taxas de infecção até 60%. O tratamento oportuna de CMV nestes pacientes é crítico para prevenir a doença de órgãos finais.
A crescente população de pacientes com HIV/AIDS em todo o mundo é outro grupo de risco que é cada vez mais propenso a infecção e doença CMV. Como o tratamento antirretroviral melhorou as taxas de sobrevivência dos pacientes com HIV, o CMV surgiu como um importante patógeno viral que afeta esta população imunocomprometida. Enquanto o tratamento antirretroviral pode controlar o HIV e restaurar alguma função imunológica, os pacientes ainda permanecem em risco para a doença de CMV. Relatórios estimam que 20-40% dos pacientes com HIV/AIDS experimentam infecção por CMV ou doença de órgãos finais envolvendo a retina, trato gastrointestinal ou pulmões em suas vidas. Com mais de 36 milhões de pessoas vivendo com HIV globalmente de acordo com a UNAIDS, a grande prevalência deste grupo de vírus continua a alimentar a necessidade de tratamento anti-CMV mais eficaz e opções profiláticas.
Driver de Mercado - Avanços Tecnológicos Facilitar Vacinas Mais Eficazes Incentivar os Desenvolvimentos da Indústria.
O progresso científico e tecnológico, especialmente nas plataformas de vacinas baseadas em ácido nucleico, está abrindo novas possibilidades para desenvolver vacinas anti-CMV seguras e eficazes. Um exemplo é o candidato vacinal MRNA-1647 da Moderna, que utiliza uma abordagem de MRNA de dois antígenos para induzir imunidade contra o complexo pentamer e envelope glicoproteína B (gB) do CMV. O complexo do Pentamer está envolvido na entrada do CMV nas células hospedeiras, enquanto o gB media a fusão entre o envelope viral e as membranas celulares hospedeiras durante a infecção. Ao segmentar esses dois principais jogadores, o mRNA-1647 visa evitar que o CMV obtenha entrada e estabelecendo infecção nas células anfitriãs.
Uma vantagem fundamental da plataforma de mRNA é a sua capacidade de impulsionar a produção in vivo de antígenos alvo em células hospedeiras, induzindo assim imunidade celular e humoral robusta contra esses antígenos. As vacinas do mRNA não contêm vírus atenuado ou inativado ao vivo, tornando-os potencialmente mais seguros do que as abordagens tradicionais da vacina. A Moderna também demonstrou a capacidade de desenvolver vacinas MRNA para outros vírus como Zika, gripe e HIV em modelos animais, apoiando a tradução do mRNA-1647 em estudos clínicos. Se comprovadamente seguro e eficaz em ensaios clínicos, um mRNA-1647 de dose única poderia fornecer proteção a longo prazo contra CMV e ajudar a reduzir sua propagação em grupos de alto risco. As inovações tecnológicas como estas estão expandindo opções para a prevenção de CMV, um grande impulsionador do crescimento do mercado.
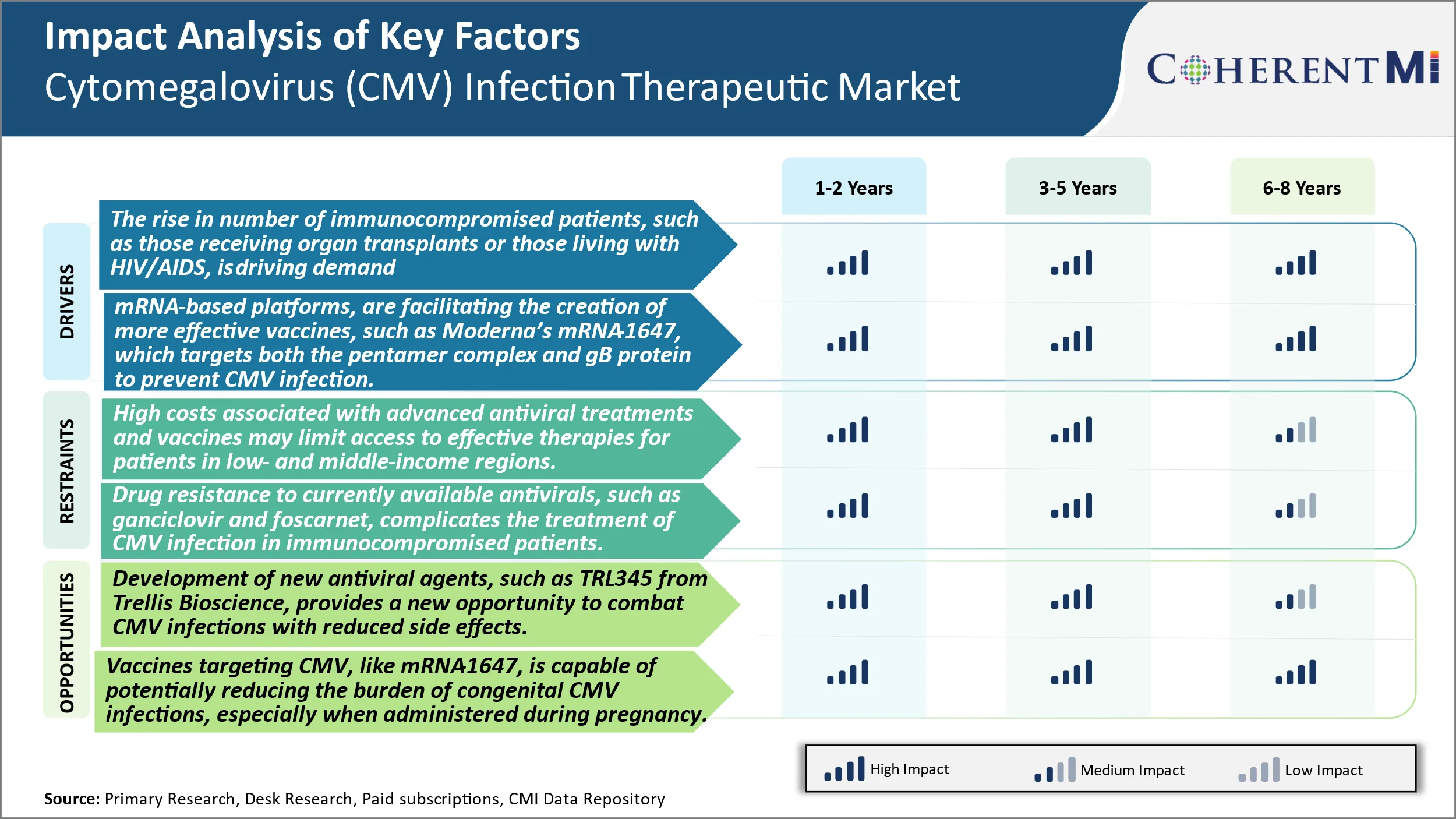
Desafio de Mercado - Altos Custos Associados a Tratamentos Antivirais Avançados e Vacinas Maio Limitar o acesso a terapias eficazes para pacientes em regiões de baixa e média renda.
O desenvolvimento de tratamentos antivirais avançados e vacinas para infecções por citomegalovírus (CMV) vem com custos consideráveis que podem potencialmente restringir o acesso ao paciente em regiões de baixa e média renda. Desenvolver novos candidatos à droga e trazê-los através do processo de ensaio clínico em aprovação regulatória envolve enormes investimentos de pesquisa e desenvolvimento por empresas farmacêuticas. Os preços de novas terapias que visam uma indicação de mercado de nicho como CMV também precisa ter em conta os altos custos para garantir retornos razoáveis. No entanto, estabelecer custos que são inacessíveis para programas de saúde pública e pacientes individuais em países em desenvolvimento significa que uma grande parte da população paciente permanece subservida. Dada a distribuição generalizada do CMV globalmente, esta disparidade no acesso ao cuidado representa um sério desafio à saúde pública. As vias e as parcerias inovadoras são necessárias para fazer novas opções de tratamento financeiramente viáveis e geograficamente acessíveis.
Oportunidade de mercado: Novos candidatos oferecem melhores opções para combater o CMV.
O desenvolvimento de novos agentes antivirais que visam o CMV oferece uma oportunidade para abordar as limitações atuais e gerenciar melhor as infecções. TRL345 da Trellis Bioscience representa um candidato promissor que atua no site de glicoproteína B conservado do vírus. Este novo mecanismo de ação pode melhorar a eficácia como a resistência é menos provável emergir em comparação com as terapias existentes. Além disso, focar em uma região altamente conservada minimiza o risco de resistência à droga em desenvolvimento devido a mutações virais ao longo do tempo e geografia. TRL345 também exibiu um perfil de efeito colateral favorável em estudos adiantados, levantando esperanças para melhor tolerabilidade. Se bem sucedido em ensaios clínicos, TRL345 pode estabelecer um novo padrão de opção de cuidado capaz de combater uma gama mais ampla de cepas CMV. Seu perfil distinto poderia expandir o potencial comercial da droga além dos rótulos atuais. Esta inovação ilustra como o R&D contínuo impulsiona o progresso e melhora as opções para enfrentar patógenos desafiadores como CMV.
Preferências dos prescritores de Cytomegalovirus (CMV) Infecção Mercado Terapêutico
CMV é comumente tratada de forma diferente com base no estado imunológico do paciente e gravidade da infecção. Para pacientes transplantados ou aqueles com sistemas imunológicos enfraquecidos, o ganciclovir (Cytovene) é o tratamento de primeira linha para infecção CMV leve a moderada. Foscarnet (Foscavir) pode ser usado em vez para pacientes que não podem tolerar ou não responder ao ganciclovir. Para casos resistentes ao tratamento ou graves, os prescritores podem usar cidofovir (Vistide) em combinação com ganciclovir ou foscarnet.
Em pacientes imunocompetentes com retinite CMV, os praticantes normalmente começam com uma dose intravenosa de ganciclovir por 2-3 semanas, seguidos por alternar para a versão oral para terapia de manutenção para evitar recaída ou progressão da doença. Valganciclovir (Valcyte), um prodrug oral de ganciclovir, também é comumente prescrito e preferido por alguns devido à sua dose oral conveniente.
Outros fatores que influenciam as escolhas do prescritor incluem custo, potenciais efeitos colaterais das drogas e limitação ou falha de tratamentos anteriores. Agentes alternativos mais recentes, como o brincidofovir (Tembexa) e o maribavir (Livtencity), entraram recentemente no mercado e podem capturar mais market share se comprovadamente mais seguro ou mais tolerável para pacientes em comparação com as opções existentes.
Análise de Opção de Tratamento de Cytomegalovirus (CMV) Infecção Mercado Terapêutico
A infecção por citomegalovírus (CMV) pode variar de assintomática para risco de vida dependendo do estado imunológico do paciente. O tratamento envolve medicação antiviral e cuidados de suporte. Para indivíduos saudáveis com sintomas leves ou sem, nenhum tratamento é necessário, pois o sistema imunológico muitas vezes pode limpar o vírus naturalmente. No entanto, para pacientes imunocomprometidos como aqueles com HIV/AIDS ou que receberam um transplante de órgãos, o CMV pode se tornar perigoso se não for tratado.
Para aqueles com doença CMV ativa, o ganciclovir é geralmente o tratamento de primeira linha. É um antiviral análogo nucleoside disponível como formas intravenosas e orais. Ele funciona para inibir a polimerase viral do DNA e parar a replicação viral. Para doença leve a moderada, valganciclovir oral também é frequentemente usado devido à sua biodisponibilidade oral melhorada em comparação com o ganciclovir.
Para pacientes que não respondem adequadamente ou não podem tolerar o ganciclovir, foscarnet é comumente usado como o agente de segunda linha. É um análogo pirophosfato fosforilado inorgânico que também impede a síntese viral do DNA. Para casos refratários ou resistentes, a forma lípido-conjugado de ganciclovir chamado cidofovir é administrada, embora tenha pior toxicidade renal.
A infecção por CMV em pacientes transplantados pode exigir terapia supressiva a longo prazo para prevenir a doença de reativação. medicação de manutenção de baixa dose com ganciclovir oral ou valganciclovir é comumente usado para isso até que a função imunológica é restaurada. O tratamento agressivo é crucial para o controle do CMV, particularmente em indivíduos imunocomprometidos, para prevenir a doença de órgãos finais e outras complicações graves.
Principais estratégias vencedoras adotadas pelos principais participantes de Cytomegalovirus (CMV) Infecção Mercado Terapêutico
Os principais jogadores como Merck & Co., Inc. e GlaxoSmithKline plc se concentraram em testes clínicos e de R&D para desenvolver novos candidatos a drogas para o tratamento de infecção CMV.
Merck & Co. lançou a droga antiviral Valganciclovir em 2001, que ainda é uma opção de tratamento padrão. Ganhou dominância no mercado através de extensos ensaios clínicos mostrando sua eficácia e segurança. Valganciclovir tornou-se a terapia de primeira linha padrão ouro, alcançando vendas anuais globais de mais de USD 500 milhões até 2010.
GlaxoSmithKline está desenvolvendo maribavir, um candidato com um novo mecanismo de ação visando a proteína quinase UL97. Em 2018, os resultados positivos da Fase 3 demonstraram que o maribavir alcançou com sucesso o ponto final primário da redução da doença CMV em comparação com a terapia antiviral convencional em receptores de transplante. Se aprovado, o maribavir será um grande avanço e capturará uma quota de mercado significativa dada a sua capacidade de atender às necessidades não satisfeitas em resistência e segurança.
Roche entrou na arena CMV através da aquisição da Argene Biosoft em 2015, obtendo acesso ao oxalato transfuranyl do candidato da droga CMV oral (TX-24), que inibe seletivamente a polimerase viral do DNA. Esta aquisição permitiu à Roche reforçar o seu pipeline anti-infeccioso. TX-24 está atualmente em estudos de fase 2 e tem potencial para ser complementar às terapias existentes.
Estes exemplos destacam como esforços constantes de R&D, ensaios clínicos bem sucedidos provando vantagens de eficácia e segurança, e aquisições para ganhar novos candidatos permitiram que os principais jogadores capturassem e defendessem liderança no mercado terapêutico CMV. O investimento sustentado em inovações que abordam necessidades médicas não atendidas provavelmente permanecerá uma estratégia fundamental para os jogadores dominarem esta área de doença.
Análise Segmental de Cytomegalovirus (CMV) Infecção Mercado Terapêutico
Insights, por tipo de drogas, a superioridade clínica dirige Valgnciclovir Market Share Dominance no Período de Previsão.
Pela Droga Tipo, Valgnciclovir é esperado para contribuir com a maior participação 41,2% em 2024 devido à sua eficácia clínica estabelecida e superioridade sobre outras alternativas terapêuticas. Valganciclovir demonstra biodisponibilidade oral significativamente maior em comparação com o ganciclovir, permitindo uma dosagem conveniente uma vez por dia. Esta facilidade de administração, juntamente com a sua capacidade de alcançar concentrações terapêuticas eficazes de drogas, tornou-o o padrão de tratamento de cuidados para infecções CMV decorrentes do transplante pós-organ. O perfil farmacocinético favorável de Valganciclovir também se traduz em melhor adesão para pacientes em comparação com várias doses diárias de outras drogas. Além disso, a valganciclovir demonstrou reduções de carga viral consistentes e significativas, juntamente com um perfil de segurança de longo prazo bem caracterizado, abrangendo mais de uma década de uso clínico. Essas vantagens terapêuticas distintas permitiram que valganciclovir dominasse a captação entre os médicos visando a supressão viral ideal e os resultados dos pacientes.

Insights, Por Aplicação, Transplantação de Órgão é o Segmento Líder no Período de Previsão.
Por Aplicação, a Transplantação de Órgãos deverá contribuir com a maior participação 51,3% em 2024, pois as terapias anti-CMV eficazes são fundamentais nesta população de pacientes. CMV continua sendo a infecção viral mais comum experimentada pelos receptores de transplante no período pós-operatório precoce devido ao seu estado imunocomprometido da supressão imunológica crônica. Infecção de CMV descontrolada apresenta riscos graves, tais como a rejeição e a perda do enxerto, bem como o aumento da susceptibilidade a infecçÃμes oportunistas. Dada a natureza sustentável do transplante de órgãos, existe uma necessidade clínica urgente de prevenir e tratar ativamente qualquer reativação CMV. As altas apostas associadas ao transplante de órgãos tornam-no um condutor influente da utilização geral de agentes anti-CMV.
Insights, pelo canal de distribuição, otimizando o acesso em configurações especializadas
Por canal de distribuição, as farmácias hospitalares devem contribuir com a maior quota de mercado em 2024. Esta disparidade ocorre como opções terapêuticas anti-CMV, como valganciclovir e ganciclovir são extensivamente administradas e monitoradas em ambientes hospitalares no início do pós-transplante. Os hospitais servem como pontos centrais de atendimento especializado para pacientes de alto risco submetidos a transplante de órgãos ou células-tronco. O cuidado é coordenado de perto em equipes médicas para otimizar a dosagem e a entrega de antivirais como parte de regimes imunossupressores multidrogas. Além disso, o tratamento ambulatório permite a administração intravenosa conveniente de medicamentos anti-CMV selecionados, como foscarnet em casos graves, não responsivos às terapias orais. No geral, o segmento hospitalar está pronto para se beneficiar de ser o ambiente preferido para iniciar e gerenciar a terapia anti-CMV em condições de risco de vida.
Informação adicional de Cytomegalovirus (CMV) Infecção Mercado Terapêutico
O citomegalovírus (CMV) representa um grande desafio de saúde pública, especialmente para indivíduos imunocomprometidos e bebês nascidos com infecções congênitas. As opções atuais de tratamento incluem antivirais como ganciclovir e foscarnet, mas estes têm limitações como resistência a drogas e toxicidade. A vacina MRNA-1647 da Moderna, atualmente em testes de fase III, mostra a promessa de prevenir infecções por CMV, induzindo a imunidade contra dois antígenos virais críticos. Além disso, as terapias baseadas em anticorpos, como TRL345, da Trellis Bioscience, visam neutralizar o vírus com alta especificidade, fornecendo opções alternativas de tratamento para infecções resistentes a drogas. O impulso global para vacinas CMV e tratamentos antivirais melhorados é alimentado pela alta carga de CMV congênita, que é uma causa principal de perda auditiva e atrasos de desenvolvimento em recém-nascidos. Enquanto o mercado de tratamentos CMV continua a crescer, os altos custos das terapias avançadas representam desafios para o acesso generalizado, particularmente nas regiões de baixa renda. À medida que a pesquisa avança, o desenvolvimento de vacinas econômicas e seguras ou terapias antivirais será crucial no controle do impacto do CMV.
Visão geral competitiva de Cytomegalovirus (CMV) Infecção Mercado Terapêutico
Os principais jogadores que operam no Cytomegalovirus (CMV) Infection Therapeutic Market incluem Moderna, Trellis Bioscience, SpyBiotech, Vical, Atara Biotherapeutics, Chimerix Inc, Pfizer Inc, Merck & Company, Johnson & Johson, Bio-Rad Laboratories Inc, e F.Hoffman La-Roche Ltd.
Cytomegalovirus (CMV) Infecção Mercado Terapêutico Líderes
- Moderna
- Biociência de Trellis
- SpyBiotech
- Vários
- Bioterapêutica de Atara
Cytomegalovirus (CMV) Infecção Mercado Terapêutico - Rivalidade Competitiva

Cytomegalovirus (CMV) Infecção Mercado Terapêutico
(Dominado por grandes players)
(Altamente competitivo com muitos jogadores.)
Desenvolvimentos recentes em Cytomegalovirus (CMV) Infecção Mercado Terapêutico
- Em maio de 2024, o MRNA-1647 de Moderna entrou Ensaios de fase III. Esta vacina visa desenvolver imunidade contra o complexo pentamer e a glicoproteína B de CMV, visando múltiplas vias envolvidas na infecção por CMV.
- Em abril de 2024, a Trellis Bioscience continuou Fase Eu testifico para TRL345, um anticorpo humano de alta afinidade que neutraliza CMV, visando a glicoproteína B, impedindo a entrada viral em células humanas.
- Em março de 2024, SpyBiotech iniciou Fase Eu testei para SPYVLP01, um candidato à vacina usando partículas semelhantes ao vírus Hepatite B para estimular uma resposta imunológica contra CMV, com o objetivo de prevenir CMV congênita e outras infecções graves em pacientes imunocomprometidos.
Cytomegalovirus (CMV) Infecção Mercado Terapêutico Segmentação
- Por tipo de droga
- Valgnciclovir
- Ganciclovir
- Cidofovir
- Foscarnet
- Por aplicação
- Transplantação de órgãos
- Transplantação de células estaminais
- Congênita CMV Infecção
- Canal de distribuição
- Farmácias Hospitalares
- Farmácias de varejo
- Farmácias Online

Gostaria de explorar a opção de comprasecções individuais deste relatório?
Perguntas Frequentes :
Quão grande é o Cytomegalovirus (CMV) Infection Therapeutic Market?
Estima-se que o Global Cytomegalovirus (CMV) Infection Therapeutic Market seja avaliado em USD 231.4 Mn em 2024 e é esperado para chegar a USD 370.2 Mn em 2031.
Qual será o CAGR do mercado terapêutico da infecção Cytomegalovirus (CMV)?
O CAGR do mercado terapêutico da infecção Cytomegalovirus (CMV) é projetado para ser de 7,10% de 2024 a 2031.
Quais são os principais fatores que impulsionam o crescimento do mercado terapêutico Cytomegalovirus (CMV) da infecção?
O número crescente de pacientes imunocomprometidos, como aqueles que recebem transplantes de órgãos ou aqueles que vivem com HIV/aids, está impulsionando a demanda por terapias mais eficazes e vacinas preventivas para CMV. Os avanços tecnológicos no desenvolvimento de vacinas, particularmente plataformas baseadas em mRNA, estão facilitando a criação de vacinas mais eficazes, como o mRNA-1647 da Moderna, que visa tanto o complexo pentamer quanto a proteína gB para prevenir a infecção por CMV são o principal fator que impulsiona o mercado terapêutico da infecção por Cytomegalovirus (CMV).
Quais são os principais fatores que dificultam o crescimento do Cytomegalovirus (CMV) Infection Therapeutic Market?
Os altos custos associados a tratamentos e vacinas antivirais avançados podem limitar o acesso a terapias eficazes para pacientes em regiões de baixa e média renda e resistência a antivirais atualmente disponíveis, tais como Ganciclovir e Foscarnet, complica o tratamento da infecção por CMV em pacientes imunocomprometidos, aumentando a necessidade de novas abordagens terapêuticas são o principal fator que dificulta o crescimento do Mercado de Infecção Cytomegalovirus (CMV).
Qual é o principal tipo de droga no Cytomegalovirus (CMV) Infection Therapeutic Market?
Valgnciclovir é o segmento principal do tipo de droga.
Quais são os principais jogadores que operam no Cytomegalovirus (CMV) Infection Therapeutic Market?
Moderna, Trellis Bioscience, SpyBiotech, Vical, Atara Biotherapeutics, Chimerix Inc, Pfizer Inc, Merck & Company, Johnson & Johson, Bio-Rad Laboratories Inc, F.Hoffman La-Roche Ltd são os principais jogadores.