Рынок лечения саркомы Юинга АНАЛИЗ РАЗМЕРОВ И ДОЛЕЙ - ТЕНДЕНЦИИ РОСТА И ПРОГНОЗЫ (2024 - 2031)
Рынок лечения саркомы Юинга сегментирован по линии лечения (локализованный, метастатический), по классу лекарств (циклофосфамид, доксорубицин, дактино....
Рынок лечения саркомы Юинга Тенденции
Драйвер рынка - Достижения в методах лечения, таких как принятие VDC / IE Регимена (Винкристин, Доксорубицин, Циклофосфамид / Ифосфамид и Этапосид) для локализованной саркомы Юинга.
Управление саркомой Юинга развивалось на протяжении многих лет с принятием мультимодальных схем лечения, которые сочетают химиотерапию с хирургией и / или лучевой терапией. Традиционно терапия первой линии включала винкристин, доксорубицин, циклофосфамид, а иногда ифосфамид и этопозид (VDC / IE). Предлагая разумные преимущества для выживания, эта традиционная химиотерапия часто ассоциировалась со значительной токсичностью, связанной с лечением.
В последнее время режим VDC/IE приобрел новый интерес благодаря умеренно улучшенной без прогрессирования и общей выживаемости, продемонстрированной европейскими и американскими клиническими исследованиями. В частности, в европейском исследовании сообщалось о 5-летней выживаемости без событий и общей выживаемости 65% и 70% соответственно с режимом VDC / IE у пациентов с локализованной саркомой Юинга. Считается, что уменьшенная доза и продолжительность ифосфамида и этапосида в этом режиме обеспечивают относительно безопасный профиль токсичности. С тех пор несколько медицинских центров приняли этот модифицированный протокол VDC / IE в качестве стандартной терапии первой линии для пациентов с неметастатической саркомой Юинга на основе ее эффективности.
Рыночный драйвер: все более широкое внедрение целевой терапии способствует развитию отрасли.
В то время как мультимодальные подходы к лечению улучшили результаты на протяжении многих лет, резистентность к лечению и рецидив остаются основными проблемами в лечении саркомы Юинга. Это привело к продолжению исследований новых целевых агентов, которые действуют через неклассические механизмы. В последние годы появилось несколько целевых методов лечения, которые предлагают пациентам больше направлений лечения, чем традиционная химиотерапия.
Примечательно, что противоопухолевый антибиотик lurbinectedin продемонстрировал многообещающую противоопухолевую активность против различных типов саркомы мягких тканей в клинических испытаниях. Основываясь на исследовании второй фазы, люрбинектин получил одобрение регулирующих органов в нескольких странах для лечения рецидивирующей саркомы Юинга. Между тем, ранние клинические исследования исследуемых препаратов, таких как секлидемстат, новый обратимый ингибитор LSD1, показали сигналы противоопухолевого ответа при рефрактерной саркоме Юинга. Такие целевые агенты, которые блокируют определенные молекулярные пути, приводящие к росту опухоли, дают новую надежду пациентам с прогрессирующим или рецидивирующим заболеванием. Несколько текущих комбинированных исследований направлены на оценку безопасности и эффективности включения этих целевых препаратов со стандартной химиотерапией. Их растущее принятие может потенциально улучшить долгосрочные результаты с течением времени.
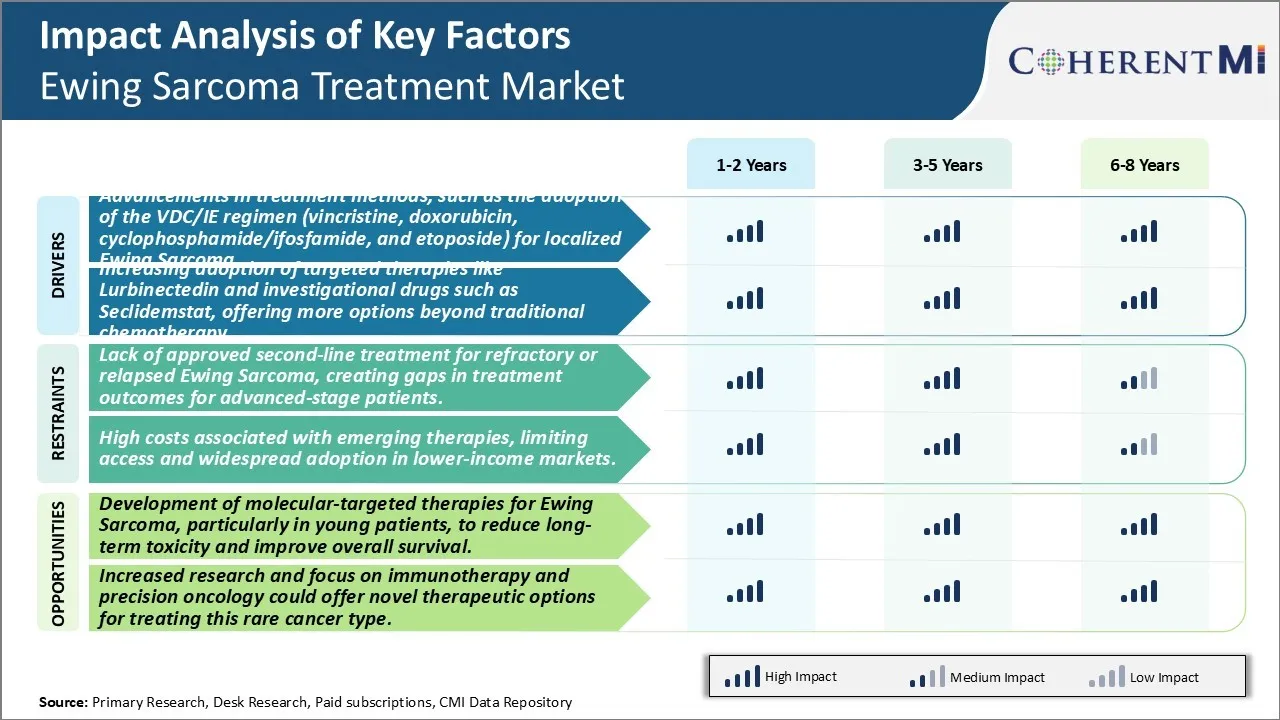
Рыночная проблема - отсутствие одобренного лечения второй линии для рефрактерной или рецидивирующей саркомы Юинга, создающей пробелы в результатах лечения для пациентов с продвинутой стадией.
Существует значительная неудовлетворенная потребность в эффективных вариантах лечения второй линии для пациентов с саркомой Юинга, у которых заболевание стало тугоплавким или рецидивировало после первой линии стандарта схем химиотерапии. Текущие протоколы лечения обычно включают интенсивную многоагентную химиотерапию, состоящую из винкристина, доксорубицина, циклофосфамида, ифосфамида и этопозида. Тем не менее, значительная часть пациентов будет испытывать прогрессирование заболевания во время или после лечения первой линии. Для этих пациентов не существует одобренных или стандартизированных методов лечения второй линии. Врачи остаются с ограниченными вариантами лечения, которые состоят в основном из прагматических клинических испытаний, оценивающих новые агенты или комбинации. Отсутствие установленного стандарта протокола лечения рецидивирующего / рефрактерного заболевания приводит к худшим результатам лечения и более низким показателям выживаемости по сравнению с пациентами, способными достичь ремиссии от фронтового лечения. Разработка одобренного FDA лечения второй линии может помочь устранить эту неудовлетворенную потребность и уменьшить пробелы в лечении, улучшив результаты для пациентов с саркомой Юинга на продвинутой стадии.
Рыночная возможность: разработка молекулярно-целевой терапии саркомы Юинга, особенно у молодых пациентов, для снижения долгосрочной токсичности и улучшения общего выживания.
Существует значительный потенциал для разработки новых молекулярно-целевых методов лечения саркомы Юинга, которые улучшают обычные схемы химиотерапии. Поскольку большинство пациентов с саркомой Юинга - дети и молодые люди, снижение токсичности, связанной с долгосрочным лечением, имеет первостепенное значение. Целенаправленные методы лечения, которые ингибируют специфические молекулярные пути, способствующие росту рака, обещают обеспечить сильную противоопухолевую активность с более благоприятными профилями безопасности по сравнению с традиционной цитотоксической химиотерапией. Недавние исследования дали представление о повторяющихся генетических мутациях и дисрегуляционных путях в саркоме Юинга, выявив новые цели для разработки лекарств. Агенты, нацеленные на программы, такие как FGF / FGFR, IGF1 / IGF1R и пути PDGF / PDGFR, показывают ранние признаки клинической пользы. Продолжение исследования целевых агентов, особенно в подгруппах пациентов, выбранных биомаркерами, может привести к вариантам, которые являются более эффективными и лучше переносимыми в долгосрочной перспективе, чем текущий стандарт схем лечения. Это может помочь максимизировать качество жизни, что особенно важно для молодых пациентов.