Cytomegalo病毒(CMV)感染治疗市场 规模与份额分析 - 成长趋势与预测 (2024 - 2031)
Cytomegalo病毒(CMV)感染治疗市场按药物类型划分(Valgnciclovir、Ganciclovir、Cidopovir、Foscarnet)、应用(组织移植、植株细胞移植、先天性CMV感染)、分配渠道(医院药房、零售药店、在线药店)、地理(北美、拉丁美洲、亚太、欧洲、中东和非洲)。 本报告提供了上述价值(百万美元)。 ....
Cytomegalo病毒(CMV)感染治疗市场 趋势
市场驱动器 -- -- 接受器官移植或艾滋病毒/艾滋病感染者等接受免疫的患者人数不断增加,正在推动为CMV提供更有效的治疗和预防疫苗。
免疫妥协患者越来越多,更容易受到CMV感染,这是改善治疗方案需求的一个主要驱动因素。 接受器官移植的患者必须服用免疫抑制药物,防止其免疫系统拒绝移植器官. 然而,这使他们容易受到感染,包括CMV。 根据研究,CMV感染在肾移植后很常见,50-80%的受感染者在第一年内会经历CMV感染. 对肺部和心脏移植病人来说,CMV感染是一个严重威胁,感染率高达60%。 及时治疗这些患者的CMV对于预防最终器官疾病至关重要.
全世界越来越多的艾滋病毒/艾滋病患者是另一个风险群体,越来越容易感染CMV和患病。 由于抗逆转录病毒治疗改善了艾滋病毒患者的存活率,CMV已成为影响这一免疫妥协人口的重要病毒病原体。 虽然抗逆转录病毒治疗能够控制艾滋病毒并恢复一些免疫功能,但病人仍然面临感染CMV疾病的风险。 报告估计,20%-40%的艾滋病毒/艾滋病患者一生中都患有涉及视网膜、胃肠道或肺的CMV感染或最终器官疾病。 根据艾滋病规划署的资料,全球有超过3 600万人感染艾滋病毒,这一病毒群体的大规模流行继续促使人们需要更有效的反CMV治疗和预防选择。
市场驱动力 - 促进更有效的疫苗的技术进步鼓励工业发展。
科技进步,特别是在以核酸为基础的疫苗平台,为研制安全有效的抗CMV疫苗开辟了新的可能性. 一个例子是Modena的MRNA-1647疫苗候选,它利用两种抗原的MRNA方法,对CMV的五聚体和信封甘油蛋白B(gB)进行免疫。 Pentamer复合体参与CMV进入宿主细胞,而gB介质在感染时病毒信封与宿主细胞膜之间的融合. mRNA-1647通过瞄准这两个关键玩家,旨在防止CMV进入并确立宿主细胞的感染.
mRNA平台的一个关键优势是它能够迅速在宿主细胞中活化地产生靶向抗原,从而诱导强健的细胞和幽默免疫力对抗这些抗原. mRNA疫苗不含活性衰减或无活性病毒,使其可能比传统疫苗方法更安全. Moderna还展示了为动物模型中的Zika,流感和艾滋病毒等其他病毒研发MRNA疫苗的能力,支持将mRNA-1647翻译成临床研究. 如果在临床试验中证明是安全和有效的,单剂量的mRNA-1647可以提供长期防范CMV的保护,并有助于遏制其在高风险群体的传播. 此类技术革新正在扩大防止CMV的选择,这是市场增长的主要动力。
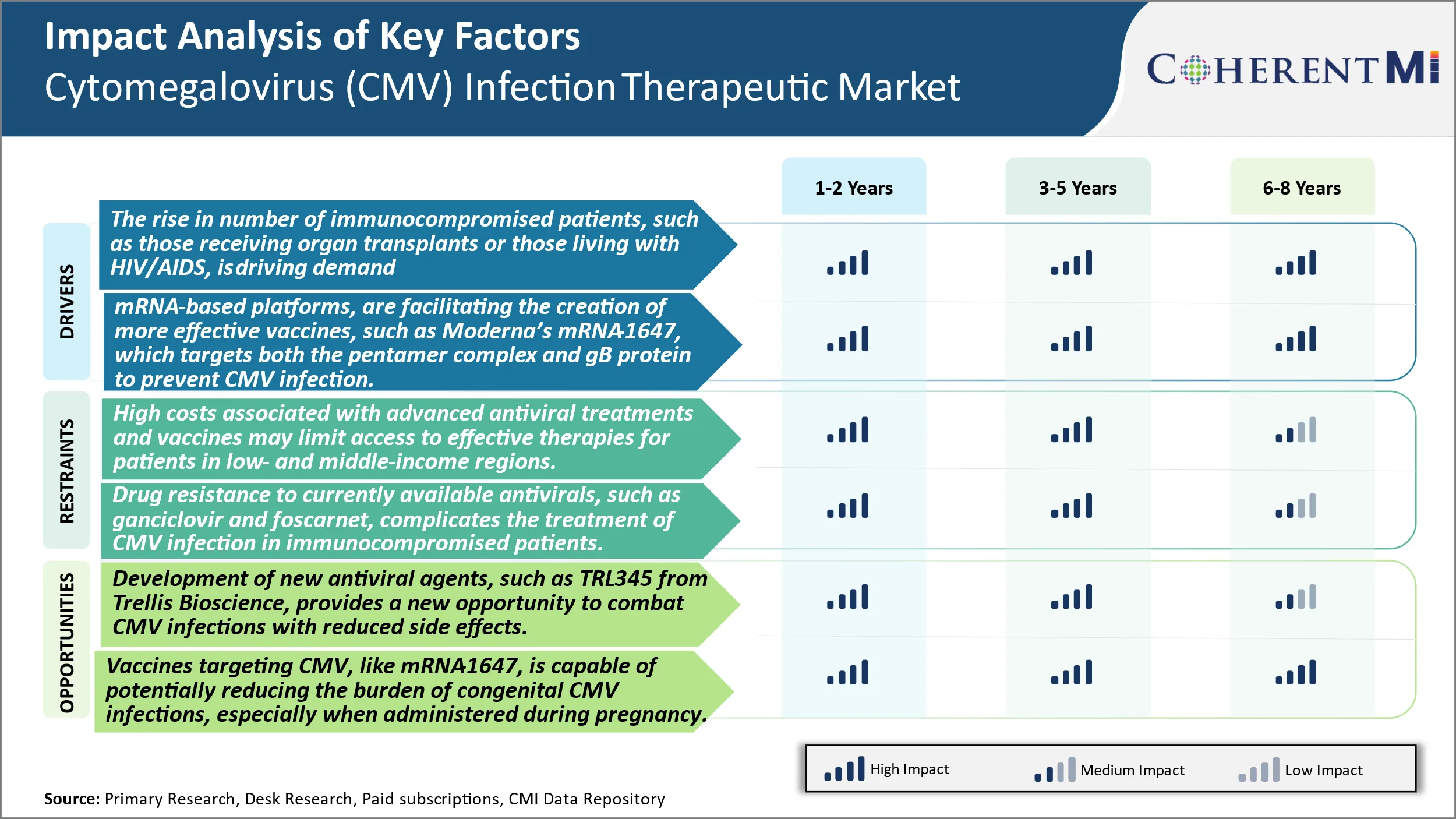
市场挑战 -- -- 与高级抗病毒治疗和疫苗有关的高昂费用可能限制中低收入地区患者获得有效治疗。
发展细胞细胞病毒感染的高级抗病毒治疗和疫苗需要大量费用,有可能限制低收入和中等收入地区的病人获得治疗。 开发新的药物候选人并将其通过临床试验程序纳入管理审批,涉及制药公司的大量研发投资。 针对诸如CMV这样的特殊市场指标的新疗法的定价还需要考虑到高成本,以确保合理的回报。 然而,在发展中国家,设定公共卫生方案和病人个人负担不起的费用意味着很大一部分病人仍然得不到足够的服务。 鉴于CMV在全球的分布,在获得护理方面的这种差距构成了严重的公共卫生挑战。 需要创新的途径和伙伴关系,使新的治疗办法在财政上可行,在地理上容易获得。
市场机会:小说候选人为打击CMV提供了更好的选择.
针对CMV开发新的抗病毒药剂,为解决目前的局限性和更好地管理感染提供了机会. Trellis Bioscience的TRL345代表着一个很有前途的候选者,在保存下来的Glyco蛋白B病毒遗址上行动. 这种新的行动机制可以提高效力,因为与现有的疗法相比,抗药性不太可能出现。 此外,注重高度保护的区域,将随着时间和地理的变异而产生抗药性的风险降至最低。 TRL345在早期研究中也表现出了有利的副作用,提高了人们对改善可容忍性的希望。 如果在临床试验中取得成功,TRL345可能会确立新的护理选择标准,能够对抗范围更广的CMV菌株. 其独特的特征可以扩大该药物的商业潜力,使其超越目前的标签。 这一创新说明,持续的研发如何推动进展,并增强应对诸如CMV等具有挑战性的病原体的备选办法。