Рынок отказов, опосредованных антителами АНАЛИЗ РАЗМЕРОВ И ДОЛЕЙ - ТЕНДЕНЦИИ РОСТА И ПРОГНОЗЫ (2024 - 2031)
Рынок отказов, опосредованных антителами, сегментируется лечением (обмен плазмой, IVIG, ингибиторы комплемента, ингибиторы протеасомы), лекарствами в ....
Рынок отказов, опосредованных антителами Размер
Размер рынка в долларах США Mn
CAGR12.64%
| Период исследования | 2024 - 2031 |
| Базовый год оценки | 2023 |
| CAGR | 12.64% |
| Концентрация рынка | High |
| Основные игроки | CSL Беринг, Ханса Биофарма AB, Viela Bio, Компания Janssen Biotech, Pfizer и среди других |
дайте нам знать!
Рынок отказов, опосредованных антителами Анализ
Рынок антител-опосредованного отторжения оценивается как 126,5 млн долларов в 2024 году Ожидается, что он достигнет 291,1 млн долларов США к 2031 году, растущие с совокупным годовым темпом роста (CAGR) 12,64% с 2024 по 2031 год. Рынок в основном обусловлен увеличением процедур трансплантации твердых органов во всем мире наряду с ростом инвестиций в разработку новых терапевтических средств для лечения опосредованного антителами отторжения после трансплантации.
Рынок отказов, опосредованных антителами Тенденции
Рыночный драйвер - увеличение количества трансплантаций органов во всем мире
Растущая осведомленность о донорстве органов в сочетании с современными хирургическими методами позволили врачам успешно проводить сложные процедуры трансплантации на регулярной основе. Это значительно увеличило общее количество трансплантаций органов, выполняемых во всем мире каждый год. Например, данные Сети по закупкам и трансплантации органов (OPTN) в Соединенных Штатах показывают, что объемы за последнее десятилетие неуклонно росли, и только в 2021 году было проведено более 40 000 трансплантаций.
Однако, несмотря на то, что донорский орган поступает от хорошо подобранного донора, всегда существует риск отторжения иммунной системой реципиента. В этом заключается роль лекарств, которые подавляют иммунную систему или мешают ее механизму отторжения. С ростом показателей трансплантации во всем мире спрос на лекарства против отторжения растет в тандеме.
Фармацевтические компании вкладывают значительные средства в разработку более эффективных и целенаправленных иммунодепрессантов, которые могут помочь улучшить результаты трансплантации. Некоторые новые агенты даже направлены на индуцирование иммунотолерантности, позволяя пациентам с трансплантацией в конечном итоге избавиться от иммуносупрессии в долгосрочной перспективе. Все эти факторы указывают на постоянно расширяющийся пул пациентов, которым потенциально могут потребоваться пожизненные лекарства против отторжения, тем самым продвигая соответствующий рынок вперед.
Драйвер рынка - Достижения в терапии, нацеленной на механизмы отказа иммунной системы
Медицинская наука продолжает развиваться быстрыми темпами, внося многочисленные полезные изменения в области трансплантологической иммунологии. Исследователи расшифровали сложные детали о том, как иммунная система распознает несамостоятельные проблемы и инициирует атаку. Фармацевтические фирмы используют иммунологические идеи посредством специальных исследований и разработок, направленных на разработку профилактических средств следующего поколения.
Некоторые примеры включают биологические препараты, ингибирующие специфические стимулирующие молекулы на иммунных клетках или антитела, нейтрализующие воспалительные цитокины, высвобождаемые во время отторжения аллотрансплантата. Клинические исследования, оценивающие эти биологические препараты, показывают эффективное подавление иммунной активации без широкого подавления, что приводит к улучшению функции трансплантата и выживанию пациентов. Другой перспективной ареной является генная терапия, при которой введение или заглушение определенных генов может помочь генерировать антиген-специфическую нереактивность или оперативную толерантность к трансплантированным органам. Ожидается, что такие целевые стратегии заменят обычные неспецифические иммунодепрессанты в долгосрочной перспективе.
Кроме того, перспективны такие технологии, как индукция толерантности к трансплантатам через смешанный химеризм. Здесь стволовые клетки костного мозга от донора переливают для установления взаимных популяций гемопоэтических клеток между донором и реципиентом. Поскольку результаты этих новых методов лечения начинают давать положительные результаты в ближайшие годы, они могут трансформировать использование противоотказных препаратов после трансплантации. Это дополнительно подтверждает сильную динамику роста для общего рынка на этом фоне.
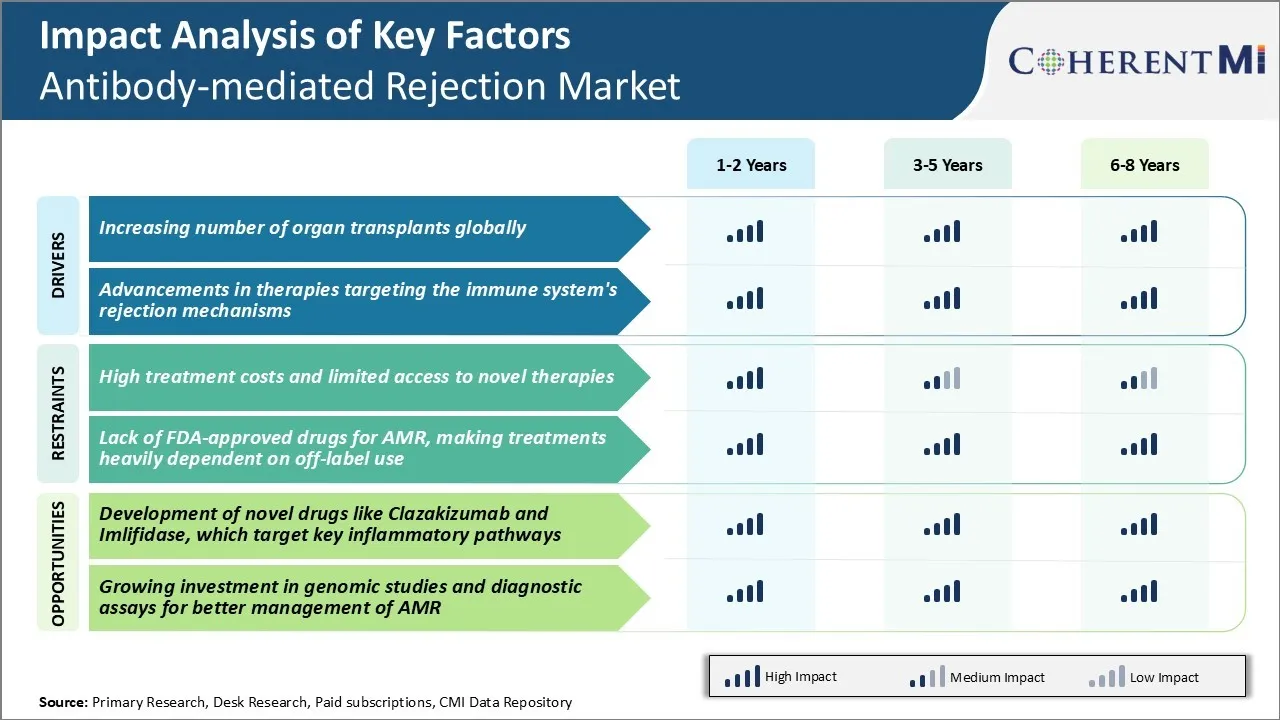
Вызов рынка: высокие затраты на лечение и ограниченный доступ к новым методам лечения
Одной из основных проблем, с которыми в настоящее время сталкивается рынок отказов от антител, является высокая стоимость лечения и ограниченный доступ к новым и новым методам лечения. Лечение отторжения, опосредованное антителами, включает использование иммуносупрессивных препаратов, таких как инфликсимаб, ритуксимаб и внутривенный иммуноглобулин, которые очень дороги для пациентов и систем здравоохранения. Среднегодовая стоимость препарата для лечения отторжения, опосредованного антителами, оценивается в диапазоне от 20 000 до более 100 000 долларов США на пациента. Кроме того, многие новые методы лечения, которые все еще находятся в разработке или недавно были одобрены, не являются широко доступными или доступными для всех пациентов. Частичное покрытие страховыми планами и системами здравоохранения делает эти новые варианты лечения недоступными для некоторых пациентов. Высокое экономическое бремя лечения отторжения, опосредованного антителами, создает трудности для более широкого доступа пациентов во всем мире и угрожает устойчивости бюджетов здравоохранения. Более широкое внедрение новых и новых методов лечения также зависит от демонстрации превосходных клинических преимуществ по сравнению с существующими вариантами, а также от успешных переговоров с плательщиками о ценах на лекарства. Эти проблемы доступа должны быть решены для улучшения результатов лечения для большего числа пациентов с отторжением, опосредованным антителами, во всем мире.
Рыночная возможность - разработка новых лекарственных средств, нацеленных на ключевые воспалительные процессы Дороги
Основная возможность на рынке отторжения, опосредованного антителами, заключается в разработке новых лекарств, которые нацелены на ключевые воспалительные пути, связанные с этим заболеванием. Например, Clazakizumab представляет собой моноклональное антитело против IL-6, которое показало перспективу в снижении острых эпизодов отторжения в клинических испытаниях. IL-6 является основным провоспалительным цитокином, вовлеченным в опосредованное антителами повреждение трансплантированных органов.
Аналогичным образом, Имлифидаза представляет собой ферментную терапию, предназначенную для ферментативного разложения IgG, которые играют центральную роль в инициировании отторжения, опосредованного антителами. В исследованиях фазы 2 Имлифидаза продемонстрировала эффективность в десенсибилизации высокочувствительных пациентов до трансплантации почек.
В качестве новых механизмов действия Клазакизумаб и Имлифидаза имеют потенциал для достижения превосходных клинических результатов по сравнению с существующими методами лечения. Их одобрение в ближайшие годы может помочь удовлетворить неудовлетворенные потребности в подгруппах пациентов с высоким уровнем антител.
Кроме того, нацеливание на новые воспалительные пути может дать варианты синергетической комбинированной терапии с иммуномодуляторами. Это дает возможность улучшить прогнозы пациентов и качество жизни.
Предпочтения врачей Рынок отказов, опосредованных антителами
Отторжение, опосредованное антителами (AMR), обычно лечится с помощью поэтапного подхода, основанного на тяжести и стадии отторжения. Для легкой AMR на ранней стадии после трансплантации, назначающие обычно начинают с повышенной иммуносупрессии с использованием лекарств, таких как такролимус (Prograf), микофенолат мофетил (CellCept) и кортикостероиды.
Если симптомы не улучшаются при усиленной исходной иммуносупрессии, назначающие могут прогрессировать лечение до терапии первой линии плазмафереза и внутривенного иммуноглобулина (IVIg). Плазмаферез используется для фильтрации покрытых антителами донорских клеток из кровообращения, в то время как IVIg обеспечивает неясные преимущества посредством иммуномодуляции. Бренды, предписанные включают Fenwal Plasma Collection System для плазмафереза и Gamunex, Octagam или Privigen для IVIg.
Для случаев, все еще не реагирующих на лечение первой линии или пациентов с более тяжелой острой AMR, врачи часто используют ритуксимаб (ритуксан) - моноклональное антитело, нацеленное на В-клетки. Эта терапия второй линии направлена на истощение клеток, продуцирующих антитела. Неответчики или те, у кого есть хроническая активная AMR, могут перейти к вариантам третьей линии, таким как бортезомиб (Velcade), ингибитор протеасомы с механистической пользой или экулизумаб (Soliris), ингибитор комплемента, нацеленный на пути воспаления.
Другие факторы, влияющие на выбор рецептора, включают профили побочных эффектов, соображения стоимости, страховое покрытие для фирменных продуктов и наличие дженериков или биоаналогов, где это применимо. Тщательный мониторинг функции почек и уровня антител также помогает определить успех лечения с течением времени.
Анализ вариантов лечения Рынок отказов, опосредованных антителами
Антитело-опосредованное отторжение (АМР) имеет три основные стадии – субклиническую, клиническую и хроническую активную АМР. Для субклинической AMR предпочтительное лечение первой линии включает использование внутривенного иммуноглобулина (IVIG). IVIG работает путем подавления производства антител и, как правило, хорошо переносится.
Для клинической АМР стандартная комбинация лечения первой линии включает плазменный обмен + IVIG + тимоглобулин/кроличий антитимоцитарный глобулин (rATG)/базиликсимаб. Плазменный обмен используется для быстрого удаления антидонорных антител из кровообращения. IVIG обеспечивает дополнительную иммуносупрессию наряду с rATG/basiliximab, которые являются мощными Т-клеточными разрушающими агентами. Эта тройная терапия направлена на одновременное уничтожение антител и подавление иммунных клеток.
В случаях, когда терапия первой линии терпит неудачу или для хронической активной AMR, используются методы лечения второй линии, такие как бортезомиб, экулизумаб или ритуксимаб. Бортезомиб является ингибитором протеасомы, который подавляет плазматические клетки, продуцирующие антитела. Eculizumab блокирует терминальную систему комплемента для предотвращения повреждения тканей от AMR. Ритуксимаб истощает В-клетки, уменьшая производство новых антител.
Для рецидивирующей или рефрактерной АМР могут использоваться агрессивные подходы, включающие комбинации вышеперечисленных препаратов. К ним относятся rATG/бортезомиб или экулизумаб/бортезомиб для достижения синергетического подавления как гуморального, так и клеточного иммунитета. Раннее выявление и быстрое лечение на каждой стадии УПП приводит к лучшим долгосрочным результатам выживаемости трансплантата.
Ключевые выигрышные стратегии, принятые ключевыми игроками Рынок отказов, опосредованных антителами
Фокус на инновационном развитии наркотиков Такие компании, как Bristol-Myers Squibb и Alexion Pharmaceuticals, вложили значительные средства в исследования и разработки новых терапевтических антител, нацеленных на конкретные пути, участвующие в AMR. Например, в 2020 году белимумаб Бристоля-Майерса Сквибба (Benlysta) получил одобрение FDA на лечение УПП у реципиентов почек.
Приобретения и партнерства Крупные игроки приобрели небольшие биотехнологии, работающие над перспективными кандидатами на лекарства от УПП, чтобы получить доступ к их трубопроводам. Например, в 2015 году Alexion приобрела Synageva для получения ингибитора комплемента C5 (ALXN1210) на клинической стадии, который показал потенциал в предотвращении AMR в испытаниях. Это укрепило портфель Алексиона.
Сосредоточьтесь на создании реальных доказательств Компании оказывают поддержку крупным продольным исследованиям и клиническим регистрам, которые помогают генерировать реальные данные о моделях лечения и результатах. Например, данные Национального реестра трансплантационной беременности, созданного при поддержке Бристоля-Майерса Сквибба, показали, что белимумаб хорошо переносился у реципиентов трансплантата, поддерживая его утверждение и принятие.
Инициативы по информированию клиницистов Образовательные программы и маркетинговые усилия помогают повысить осведомленность нефрологов, трансплантологов и иммунологов о роли конкретных целей, таких как C5a, в патогенезе УПП и полезности новых лекарств. Это помогло Bristol-Myers Squibb получить преимущество первого погрузчика с одобрением поста belimumab.
Сегментарный анализ Рынок отказов, опосредованных антителами
Проницательность, путем лечения: Широко распространенная доступность и клиническая эффективность приводят к принятию плазменного обмена
Ожидается, что в 2024 году на долю плазменного обмена будет приходиться 35,3% рынка отторжения, опосредованного антителами, благодаря его широкой доступности и доказанной клинической эффективности. Технология Plasma Exchange хорошо зарекомендовала себя в больницах и центрах трансплантации по всему миру. Оборудование и одноразовые материалы, необходимые для плазмообмена, стандартизированы и производятся несколькими крупными компаниями-производителями медицинских изделий, что обеспечивает надежный доступ.
Кроме того, плазменный обмен имеет долгую историю клинического использования для лечения острого отторжения трансплантата, опосредованного антителами, с многочисленными исследованиями, демонстрирующими улучшение выживаемости трансплантата при использовании в качестве варианта лечения первой линии. Его способность быстро очищать патогенные антитела от кровообращения путем селективной замены плазмы представляет собой логический и физиологический подход.
Процедура также хорошо переносится с относительно безопасным профилем побочных эффектов. Кроме того, опыт плазменного обмена среди клиницистов, выполняющих трансплантацию почек, обеспечивает повышенное знакомство и комфорт при назначении. Комбинированные факторы широкой доступности, клинические данные, сеть поставщиков, практичность использования и знакомство среди медицинских работников сделали Plasma Exchange лидером в сегменте терапии удаления антител.

Insights, By Drugs in Development: Promising Efficacy Data Positions Clazakizumab Atop Antibody-mediating Rejection Drugs in Development
С точки зрения лекарств в разработке, Clazakizumab вносит наибольшую долю рынка отторжения, опосредованного антителами, благодаря новым данным об эффективности клинических испытаний. Клазакизумаб представляет собой моноклональное антитело, которое ингибирует провоспалительный цитокин интерлейкин-6 (IL-6). Помимо иммуномодулирующих эффектов, доклинические исследования показывают, что IL-6 играет непосредственную роль в стимулировании производства антител. Продолжающееся клиническое исследование фазы 2 оценивает Clazakizumab для предотвращения отторжения, опосредованного антителами, у реципиентов трансплантации почки.
Предварительные данные, представленные на недавней научной конференции, продемонстрировали снижение уровня донор-специфических антител и субклинические события отторжения по сравнению с плацебо. Если это подтвердится в полных результатах исследования, это может установить Клазакизумаб в качестве первого системного препарата, показанного эффективным для профилактики отторжения, опосредованного антителами, в рандомизированном контролируемом исследовании.
Перспективные результаты на сегодняшний день вызвали значительный интерес в сообществе трансплантологов и привлекли внимание инвесторов к этому первоклассному механизму. За исключением каких-либо проблем безопасности в последующих испытаниях, Clazakizumab, по-видимому, имеет хорошие шансы стать ведущим терапевтическим препаратом в этом сегменте.
По терапевтическому подходу: превосходная специфичность цели приводит к моноклональным антителам в терапевтических подходах, основанных на отказе от антител
С точки зрения терапевтического подхода, моноклональные антитела обеспечивают наибольшую долю рынка благодаря своей изысканной специфичности. В отличие от обычной иммуносупрессивной терапии, моноклональные антитела позволяют селективную блокаду молекул, участвующих в производстве антител и ответе, а не системное подавление иммунитета.
Например, антитела против CD20 избирательно истощают В-клетки, ответственные за секрецию аллоантител, не полностью отменяя гуморальный иммунитет. Ингибиторы комплемента обеспечивают менее точный подход, широко ингибируя несколько путей активации комплемента по всему телу.
Способность моноклональных антител определять ключевых игроков в каскаде отторжения, сохраняя при этом нецелевой иммунитет, делает их особенно подходящими для проблем с трансплантацией, опосредованной антителами. Препараты, такие как Белимумаб, нацеленные на BAFF, оцениваются для предотвращения восстановления сенсибилизированных донорских антител пациентов.
Кроме того, во многих центрах трансплантации используются препараты IVIG с низкой дозой, обогащенные анти-CD20, для истощения долгоживущих плазматических клеток в рефрактерных случаях. Точность этих целевых биологических методов лечения в сочетании с улучшением методов производства рекомбинантных антител продолжает вызывать интерес и долю сегмента для моноклональных антител в лечении отторжения, опосредованного антителами.
Дополнительные идеи Рынок отказов, опосредованных антителами
- AMR представляет собой спектр состояний, сосуществующих с T-клеточным отторжением, часто приводящим к потере аллотрансплантата и характеризующимся специфическими для донора антителами.
- США возглавляют случаи отторжения, опосредованные антителами, в 7MM, что составляет более 60% от общего числа случаев.
- Случаи трансплантации почек, легких и печени были основными причинами случаев отторжения, опосредованных антителами, в 7MM в 2023 году.
- Во Франции было наибольшее количество случаев отторжения, опосредованных антителами, в EU4.
- Отторжение, опосредованное антителами, затрагивает примерно 5-7% всех трансплантаций почек, причем острая АМР особенно трудно поддается лечению из-за изменчивости реакции пациента. Отсутствие стандартизированных руководящих принципов лечения еще больше усложняет управление пациентами, при этом методы лечения в значительной степени основаны на использовании в других областях медицины.
Обзор конкурентов Рынок отказов, опосредованных антителами
Основные игроки, работающие на рынке антител-опосредованного отторжения, включают CSL Behring, Hansa Biopharma AB, Viela Bio, Janssen Biotech, Pfizer, Sanofi, HI-Bio и Horizon Therapeutics.
Рынок отказов, опосредованных антителами Лидеры
- CSL Беринг
- Ханса Биофарма AB
- Viela Bio
- Компания Janssen Biotech
- Pfizer
Рынок отказов, опосредованных антителами - Конкурентное соперничество

Рынок отказов, опосредованных антителами
(Доминируют крупные игроки)
(Высококонкурентный с большим количеством игроков.)
Последние разработки в Рынок отказов, опосредованных антителами
- В марте 2024 года Human Immunology Biosciences (HI-Bio) объявила, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) предоставило орфанный препарат для лечения отторжения, опосредованного антителами (AMR) у реципиентов трансплантации почки. Это обозначение является важным шагом для развития фельцартамаба, моноклонального антитела, которое нацелено на CD38+ плазматические клетки, которые играют ключевую роль в AMR. Обозначение сиротских наркотиков помогает продвигать разработку методов лечения редких заболеваний, предлагая такие стимулы, как налоговые льготы и эксклюзивность рынка после одобрения.
- В январе 2024 года Ханса Биофарма AB опубликовала положительные результаты своих исследований Imlifidase, сосредоточившись на острых случаях УПП, когда обычные методы лечения не увенчались успехом, что ознаменовало прорыв в вариантах лечения реципиентов трансплантата. Испытания показали, что имлифидаза значительно снижает донор-специфические антитела (DSA) в течение пяти дней после лечения, что ознаменовало значительный прорыв для реципиентов трансплантата, столкнувшихся с отторжением. Это особенно важно для пациентов с AMR, ведущей причиной недостаточности трансплантата, поскольку в настоящее время нет утвержденных методов лечения этого состояния. Обнадеживающие результаты этих испытаний фазы 2 показали, что имлифидаза была более эффективной и быстрой при снижении DSA по сравнению с традиционными процедурами плазмообмена.
- В мае 2023 года CSL Беринг продвинул Clazakizumab в III фазу клинических испытаний, чтобы исследовать его потенциал в лечении хронического активного отторжения, опосредованного антителами (AMR) у реципиентов трансплантации почки. Это важная область исследований, потому что АМР является основной причиной поздней потери трансплантата почки, и текущие варианты лечения ограничены.
- В октябре 2018 года Управление по контролю за продуктами и лекарствами США (FDA) предоставило Fast Track Designation имлифидазе, препарату, разработанному Hansa Biopharma, для исследования его использования в трансплантации. В частности, имлифидаза изучается на предмет ее потенциала для обеспечения трансплантации почек у пациентов с высокой чувствительностью путем инактивации вредных антител, которые в противном случае могут вызвать отторжение органов.
Рынок отказов, опосредованных антителами Сегментация
- Лечение
- Плазменный обмен
- IVIG
- Ингибиторы дополнения
- Ингибиторы протеасом
- Наркотики в развитии
- Клазакизумаб
- Имлифидаза
- По терапевтическому подходу
- моноклональный Антитела
- Ингибиторы дополнения
- По типу пациента
- Пресенсибилизированные получатели трансплантации
- Острые пациенты с AMR

Хотите изучить возможность покупкиотдельные разделы этого отчета?
Часто задаваемые вопросы :
Насколько велик рынок антител-опосредованного отторжения?
Рынок антител-опосредованного отторжения оценивается в 126,5 млн долларов США в 2024 году и, как ожидается, достигнет 291,1 млн долларов США к 2031 году.
Каковы ключевые факторы, препятствующие росту рынка отторжения, опосредованного антителами?
Высокие затраты на лечение, ограниченный доступ к новым методам лечения и отсутствие одобренных FDA препаратов для лечения УПП, что делает лечение в значительной степени зависимым от немаркированного использования, являются основными факторами, препятствующими росту рынка отторжения, опосредованного антителами.
Каковы основные факторы, влияющие на рост рынка отторжения, опосредованного антителами?
Увеличение числа трансплантаций органов во всем мире и достижения в терапии, направленной на механизмы отторжения иммунной системы, являются основными факторами, определяющими рынок отторжения, опосредованного антителами.
Что является ведущим лечением на рынке отторжения, опосредованного антителами?
Ведущим сегментом лечения является плазменный обмен.
Какие основные игроки работают на рынке отторжения, опосредованного антителами?
CSL Behring, Hansa Biopharma AB, Viela Bio, Janssen Biotech, Pfizer, Sanofi, HI-Bio и Horizon Therapeutics являются основными игроками.
Каким будет CAGR рынка антител-опосредованного отторжения?
Прогнозируется, что CAGR рынка антител-опосредованного отторжения составит 12,64% с 2024 по 31 год.