Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок АНАЛИЗ РАЗМЕРОВ И ДОЛЕЙ - ТЕНДЕНЦИИ РОСТА И ПРОГНОЗЫ (2024 - 2031)
Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок сегментирован по типу лекарств (Valgnciclovir, Ganciclovir, Cidofovir, Foscarnet), по применению (органическая трансплантация, трансплантация стволовых клеток, врожденная инфекция ЦМВ), по каналу распространения (больничные аптеки, розничные аптеки, онлайн-аптеки), по географии (Северная Америка, Латинская Америка, Азиатско-Тихоокеанский регион, Европа, Ближний Восток и Африка). В отчете предлагается стоимость (в миллионах долларов США) для вышеупомянутого.
Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок Размер
Размер рынка в долларах США Mn
CAGR7.10%
| Период исследования | 2024 - 2031 |
| Базовый год оценки | 2023 |
| CAGR | 7.10% |
| Концентрация рынка | Medium |
| Основные игроки | Модерн, Trellis Bioscience, SpyBiotech, Викальный, Atara Biotherapeutics и среди других |
дайте нам знать!
Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок Анализ
Глобальный рынок терапевтической терапии цитомегаловируса (ЦМВ) оценивается как $231,4 млн в 2024 году Ожидается, что он достигнет 370,2 млн долларов США к 2031 году, растущие с совокупным годовым темпом роста (CAGR) 7,10% с 2024 по 2031 год. Рынок был в основном обусловлен ростом заболеваемости ЦМВ-инфекцией среди младенцев и больных СПИДом, а также наличием препаратов на поздних стадиях, которые, вероятно, поступят на рынок в ближайшие годы.
За последние несколько лет рыночная тенденция показала устойчивый и постепенный рост. Недавние исследования и партнерские отношения между компаниями работали над улучшением диагностических методов и терапевтических разработок для ЦМВ-инфекции. Кроме того, рост осведомленности о гигиенической практике и профилактике инфекций положительно повлиял на объем рынка. Ожидается, что дальнейшие инновации для обеспечения более широких вариантов лечения продолжат стимулировать рынок в течение прогнозируемого периода.
Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок Тенденции
Растущее число пациентов с ослабленным иммунитетом, таких как те, кто получает трансплантаты органов или те, кто живет с ВИЧ / СПИДом, стимулирует спрос на более эффективные методы лечения и профилактические вакцины для ЦМВ.
Растущее число пациентов с ослабленным иммунитетом, которые более восприимчивы к инфекции ЦМВ, является ключевым фактором спроса на улучшенные варианты лечения. Пациенты, которые получают трансплантацию органов, должны принимать иммунодепрессанты, чтобы предотвратить отторжение пересаженного органа их иммунной системой. Однако это делает их уязвимыми для инфекций, включая ЦМВ. Согласно исследованиям, ЦМВ-инфекция распространена после трансплантации почки, причем 50-80% реципиентов испытывают ЦМВ-инфекцию в течение первого года. Для пациентов с трансплантацией легких и сердца, инфекция ЦМВ является серьезной угрозой, с частотой заражения до 60%. Своевременное лечение ЦМВ у этих пациентов имеет решающее значение для предотвращения заболевания конечных органов.
Растущее число пациентов с ВИЧ/СПИДом во всем мире является еще одной группой риска, которая все чаще подвержена инфекции и заболеванию ЦМВ. Поскольку антиретровирусное лечение улучшило показатели выживаемости пациентов с ВИЧ, ЦМВ стал важным вирусным патогеном, влияющим на эту популяцию с ослабленным иммунитетом. В то время как антиретровирусное лечение может контролировать ВИЧ и восстанавливать некоторые иммунные функции, пациенты по-прежнему подвергаются риску заболевания ЦМВ. По оценкам, 20-40% пациентов с ВИЧ / СПИДом испытывают ЦМВ-инфекцию или заболевание конечных органов с участием сетчатки, желудочно-кишечного тракта или легких в течение своей жизни. По данным ЮНЭЙДС, более 36 миллионов человек во всем мире живут с ВИЧ, и большая распространенность этой вирусной группы продолжает подпитывать потребность в более эффективном лечении и профилактике ЦМВ.
Драйвер рынка - технологические достижения, способствующие более эффективным вакцинам, стимулируют развитие отрасли.
Научно-технический прогресс, особенно на платформах вакцин на основе нуклеиновых кислот, открывает новые возможности для разработки безопасных и эффективных вакцин против ЦМВ. Одним из примеров является кандидат на вакцину MRNA-1647 от Moderna, который использует двухантигенный подход MRNA для индуцирования иммунитета как к пентамеровому комплексу, так и к гликопротеину оболочки B (gB) ЦМВ. Пентамерный комплекс участвует в проникновении CMV в клетки-хозяева, в то время как gB опосредует слияние между вирусной оболочкой и мембранами клеток-хозяев во время инфекции. Нацеливаясь на этих двух ключевых игроков, мРНК-1647 стремится предотвратить проникновение ЦМВ в клетки-хозяева.
Ключевым преимуществом платформы мРНК является ее способность стимулировать in vivo производство целевых антигенов в клетках-хозяевах, тем самым вызывая надежный клеточный и гуморальный иммунитет против этих антигенов. Вакцины мРНК не содержат живого ослабленного или инактивированного вируса, что делает их потенциально более безопасными, чем традиционные методы вакцинации. Moderna также продемонстрировала способность разрабатывать вакцины МРНК для других вирусов, таких как Зика, грипп и ВИЧ, на животных моделях, поддерживая перевод мРНК-1647 в клинические исследования. Если доказана безопасность и эффективность в клинических испытаниях, однократная доза мРНК-1647 может обеспечить долгосрочную защиту от ЦМВ и помочь обуздать его распространение в группах высокого риска. Подобные технологические инновации расширяют возможности профилактики ЦМВ, что является основным фактором роста рынка.
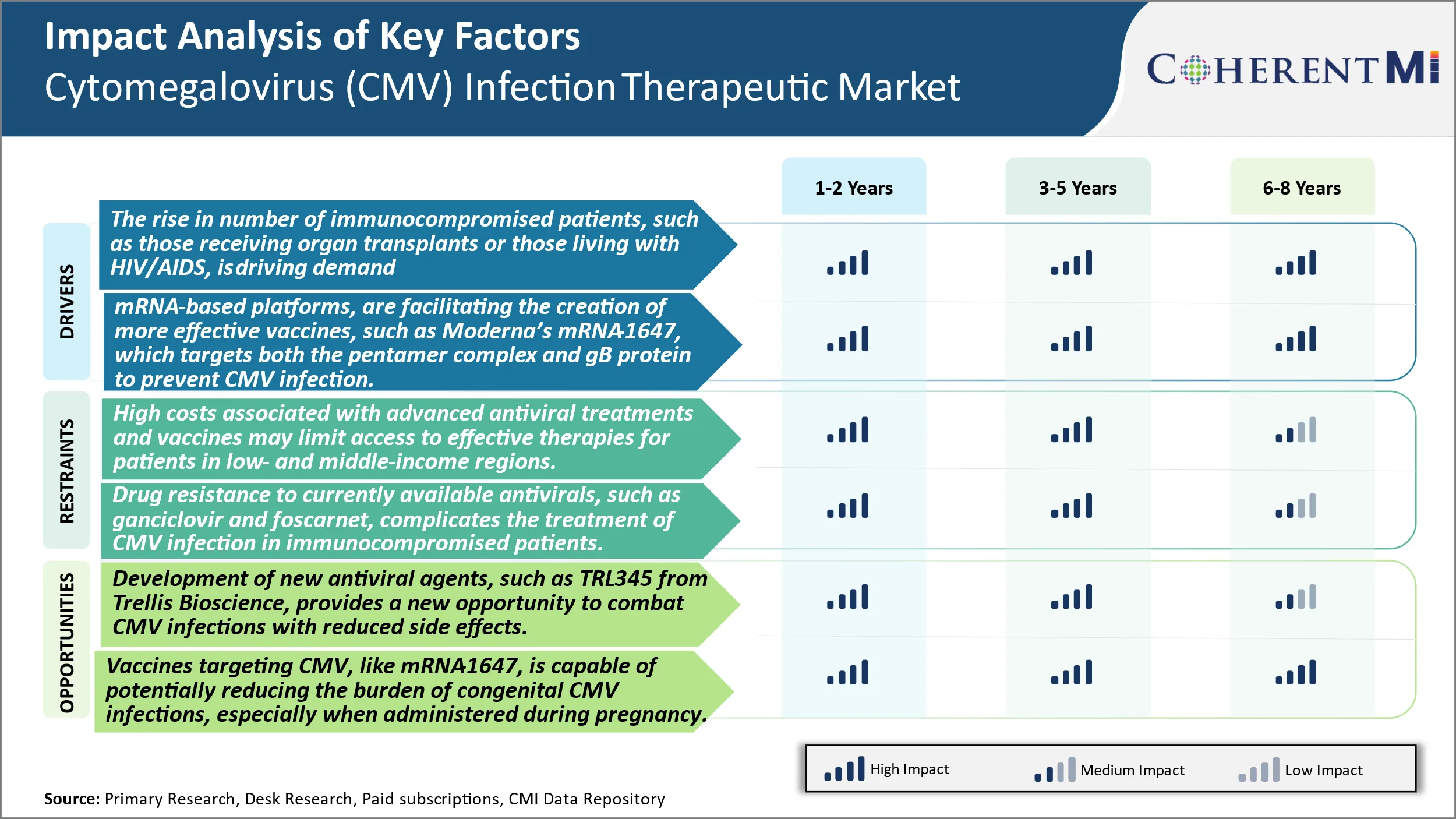
Высокие затраты, связанные с передовыми противовирусными препаратами и вакцинами, могут ограничить доступ к эффективной терапии для пациентов в регионах с низким и средним уровнем дохода.
Разработка передовых противовирусных методов лечения и вакцин против инфекций цитомегаловируса (ЦМВ) сопряжена со значительными затратами, которые потенциально могут ограничить доступ пациентов в регионах с низким и средним уровнем дохода. Разработка новых кандидатов на лекарственные препараты и их внедрение в процесс клинических испытаний для утверждения регулирующими органами предполагает огромные инвестиции фармацевтических компаний в исследования и разработки. Цена новых методов лечения, ориентированных на нишевые рыночные показатели, такие как ЦМВ, также должна учитывать высокие затраты для обеспечения разумной прибыли. Однако установление расходов, которые недоступны для программ общественного здравоохранения и отдельных пациентов в развивающихся странах, означает, что значительная часть населения остается недостаточно обслуживаемой. Учитывая широкое распространение ЦМВ во всем мире, это неравенство в доступе к медицинской помощи представляет серьезную проблему для общественного здравоохранения. Для того чтобы новые варианты лечения были финансово жизнеспособными и географически доступными, необходимы инновационные пути и партнерские отношения.
Рыночная возможность: новые кандидаты предлагают улучшенные варианты борьбы с ЦМВ.
Разработка новых противовирусных средств, нацеленных на ЦМВ, дает возможность устранить существующие ограничения и лучше управлять инфекциями. Trellis Bioscience TRL345 представляет собой многообещающий кандидат, который действует на консервативный гликопротеин B-сайт вируса. Этот новый механизм действия может повысить эффективность, поскольку резистентность менее вероятна по сравнению с существующими методами лечения. Кроме того, сосредоточение внимания на высококонсервативной области сводит к минимуму риск развития лекарственной устойчивости из-за вирусных мутаций с течением времени и географии. В ранних исследованиях TRL345 также продемонстрировал благоприятный профиль побочных эффектов, что породило надежды на улучшение переносимости. В случае успеха в клинических испытаниях TRL345 может установить новый стандарт лечения, способный бороться с более широким спектром штаммов ЦМВ. Его отличительный профиль может расширить коммерческий потенциал препарата за пределы существующих этикеток. Это нововведение иллюстрирует, как непрерывные исследования и разработки способствуют прогрессу и расширяют возможности для борьбы со сложными патогенами, такими как ЦМВ.
Предпочтения врачей Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
ЦМВ обычно лечится по-разному в зависимости от иммунного статуса пациента и тяжести инфекции. Для пациентов с трансплантацией или пациентов с ослабленной иммунной системой ганцикловир (цитовен) является первой линией лечения от легкой до умеренной инфекции ЦМВ. Фоскарнет (Фоскавир) может использоваться вместо этого для пациентов, которые не переносят или не реагируют на ганцикловир. Для резистентных к лечению или тяжелых случаев, назначающие могут использовать лидофовир (Вистид) в сочетании с ганцикловиром или фоскарнетом.
У иммунокомпетентных пациентов с ретинитом ЦМВ практикующие обычно начинают с внутривенной дозы ганцикловира в течение 2-3 недель, а затем переходят на пероральную версию для поддерживающей терапии, чтобы предотвратить рецидив или прогрессирование заболевания. Валганцикловир (Valcyte), пероральный пролекарство ганцикловира, также обычно назначают и предпочитают некоторые из-за его удобного перорального дозирования.
Другие факторы, влияющие на выбор рецептора, включают стоимость, потенциальные побочные эффекты лекарств и ограничение или неудачу предыдущих процедур. Новые альтернативные агенты, такие как бринцидофовир (Tembexa) и марибавир (Livtencity), недавно вышли на рынок и могут захватить большую долю рынка, если они окажутся более безопасными или более терпимыми для пациентов по сравнению с существующими вариантами.
Анализ вариантов лечения Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
Цитомегаловирусная (ЦМВ) инфекция может варьироваться от бессимптомной до опасной для жизни в зависимости от иммунного статуса пациента. Лечение включает противовирусные препараты и поддерживающую помощь. Для здоровых людей с легкими или без симптомов не требуется никакого лечения, так как иммунная система часто может естественным образом очистить вирус. Однако для пациентов с ослабленным иммунитетом, таких как ВИЧ / СПИД или получивших трансплантацию органов, ЦМВ может стать опасным, если его не лечить.
Для людей с активным заболеванием ЦМВ ганцикловир обычно является лечением первой линии. Это нуклеозидный аналоговый противовирусный препарат, доступный как внутривенно, так и перорально. Он работает, чтобы ингибировать вирусную ДНК-полимеразу и остановить репликацию вируса. При легкой и умеренной форме заболевания оральный валганцикловир также часто используется из-за его улучшенной оральной биодоступности по сравнению с ганцикловиром.
Для пациентов, которые не реагируют адекватно или не переносят ганцикловир, фоскарнет обычно используется в качестве агента второй линии. Это неорганический фосфорилированный аналог пирофосфата, который также предотвращает синтез вирусной ДНК. Для огнеупорных или резистентных случаев вводят липид-конъюгированную форму ганцикловира, называемую лидофовиром, хотя она имеет худшую почечную токсичность.
Инфекция ЦМВ у пациентов с трансплантацией может потребовать длительной супрессивной терапии для предотвращения реактивации заболевания. Низкая доза поддерживающего лекарства с пероральным ганцикловиром или валганцикловиром обычно используется для этого до восстановления иммунной функции. Агрессивное лечение имеет решающее значение для контроля ЦМВ, особенно у людей с ослабленным иммунитетом, для предотвращения заболеваний конечных органов и других серьезных осложнений.
Ключевые выигрышные стратегии, принятые ключевыми игроками Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
Ведущие игроки, такие как Merck & Co., Inc. и GlaxoSmithKline plc, сосредоточились на НИОКР и клинических испытаниях для разработки новых препаратов для лечения инфекции ЦМВ.
В 2001 году Merck & Co. выпустила противовирусный препарат Валганцикловир, который по-прежнему является стандартным вариантом лечения. Он завоевал господство на рынке благодаря обширным клиническим испытаниям, демонстрирующим его эффективность и безопасность. Валганцикловир стал золотым стандартом терапии первой линии, достигнув глобальных годовых продаж более 500 миллионов долларов США к 2010 году.
GlaxoSmithKline разрабатывает марибавир, кандидат с новым механизмом действия, нацеленным на протеинкиназу UL97. В 2018 году положительные результаты фазы 3 показали, что марибавир успешно достиг первичной конечной точки снижения заболеваемости ЦМВ по сравнению с обычной противовирусной терапией у реципиентов трансплантата. В случае одобрения марибавир станет крупным шагом вперед и займет значительную долю рынка, учитывая его способность удовлетворять неудовлетворенные потребности в сопротивлении и безопасности.
Roche вышла на арену CMV путем приобретения Argene Biosoft в 2015 году, получив доступ к пероральному препарату CMV-кандидату трансфуранилоксалата (TX-24), который избирательно ингибирует вирусную ДНК-полимеразу. Это приобретение позволило «Рош» укрепить свой антиинфекционный трубопровод. TX-24 в настоящее время находится в фазе 2 исследований и может дополнять существующие методы лечения.
Эти примеры показывают, как постоянные исследования и разработки, успешные клинические испытания, доказывающие преимущества эффективности и безопасности, а также приобретения новых кандидатов позволили крупным игрокам захватить и защитить лидерство на терапевтическом рынке ЦМВ. Устойчивые инвестиции в инновации, направленные на удовлетворение неудовлетворенных медицинских потребностей, вероятно, останутся ключевой стратегией для игроков, чтобы доминировать в этой области болезни.
Сегментарный анализ Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
Проницательность, по типу лекарств, клиническое превосходство приводит к Вальгнцикловиру Доминирование на рынке в прогнозный период.
Наркотики Ожидается, что в 2024 году доля Вальнгцикловира достигнет 41,2% из-за его клинической эффективности и превосходства над другими терапевтическими альтернативами. Вальганцикловир демонстрирует значительно более высокую биодоступность полости рта по сравнению с ганцикловиром, что позволяет применять его один раз в день. Эта простота введения в сочетании с его способностью достигать терапевтически эффективных концентраций лекарств сделала его стандартом лечения инфекций ЦМВ, возникающих после трансплантации органов. Благоприятный фармакокинетический профиль Вальганцикловира также приводит к улучшению приверженности пациентов по сравнению с несколькими ежедневными дозами других лекарств. Кроме того, валганцикловир продемонстрировал последовательное и значимое снижение вирусной нагрузки наряду с хорошо характеризованным долгосрочным профилем безопасности, охватывающим более десяти лет клинического использования. Эти различные терапевтические преимущества позволили валганцикловиру доминировать среди врачей, стремящихся к оптимальному подавлению вирусов и результатам лечения пациентов.

По применению трансплантация органов является ведущим сегментом в прогнозируемый период.
Ожидается, что в 2024 году доля трансплантации органов будет самой высокой — 51,3%, поскольку эффективная терапия против ЦМВ имеет первостепенное значение в этой популяции пациентов. ЦМВ остается наиболее распространенной вирусной инфекцией, испытываемой реципиентами трансплантата в раннем послеоперационном периоде из-за их иммунокомпрометированного состояния от хронического подавления иммунитета. Неконтролируемая инфекция ЦМВ представляет серьезные риски, такие как отторжение трансплантата и потеря, а также повышенная восприимчивость к оппортунистическим инфекциям. Учитывая жизнеустойчивый характер трансплантации органов, существует неотложная клиническая необходимость активно предотвращать и лечить любую реактивацию ЦМВ. Высокие ставки, связанные с трансплантацией органов, делают его влиятельным фактором использования анти-ЦМВ-агентов в целом.
Insights, By Distribution Channel, Оптимизация доступа в специализированных настройках
По каналу дистрибуции больничные аптеки, как ожидается, внесут наибольшую долю рынка в 2024 году. Это несоответствие происходит, поскольку терапевтические варианты против ЦМВ, такие как валганцикловир и ганцикловир, широко применяются и контролируются в больницах на ранних этапах после трансплантации. Больницы служат центральными пунктами специализированной помощи пациентам высокого риска, перенесшим трансплантацию органов или стволовых клеток. Уход тесно координируется между медицинскими командами для оптимизации дозирования и доставки противовирусных препаратов в рамках многолекарственных иммуносупрессивных схем. Кроме того, стационарное лечение позволяет удобно вводить внутривенно некоторые анти-ЦМВ препараты, такие как фоскарнет, в тяжелых случаях, не реагирующих на оральную терапию. В целом, больничный сегмент готов извлечь выгоду из того, что он является предпочтительной средой для инициирования и управления анти-ЦМВ-терапией в опасных для жизни условиях.
Дополнительные идеи Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
Цитомегаловирус (ЦМВ) представляет собой серьезную проблему общественного здравоохранения, особенно для людей с ослабленным иммунитетом и младенцев, родившихся с врожденными инфекциями. Текущие варианты лечения включают противовирусные препараты, такие как ганцикловир и фоскарнет, но они имеют ограничения, такие как лекарственная устойчивость и токсичность. Вакцина MRNA-1647 от Moderna, которая в настоящее время находится в испытаниях III фазы, демонстрирует перспективность в предотвращении инфекций ЦМВ, вызывая иммунитет против двух критических вирусных антигенов. Кроме того, терапия на основе антител, такая как TRL345 от Trellis Bioscience, направлена на нейтрализацию вируса с высокой специфичностью, предоставляя альтернативные варианты лечения лекарственно-устойчивых инфекций. Глобальный толчок для вакцин против ЦМВ и улучшенных противовирусных методов лечения подпитывается высоким бременем врожденного ЦМВ, который является ведущей причиной потери слуха и задержки развития у новорожденных. В то время как рынок лечения ЦМВ продолжает расти, высокие затраты на передовые методы лечения создают проблемы для широкого доступа, особенно в регионах с низким уровнем дохода. По мере развития исследований разработка экономически эффективных и безопасных вакцин или противовирусных препаратов будет иметь решающее значение для контроля воздействия ЦМВ.
Обзор конкурентов Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
Основными игроками, работающими на рынке терапии инфекций цитомегаловируса (CMV), являются Moderna, Trellis Bioscience, SpyBiotech, Vical, Atara Biotherapeutics, Chimerix Inc, Pfizer Inc, Merck & Company, Johnson & Johson, Bio-Rad Laboratories Inc и F.Hoffman La-Roche Ltd.
Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок Лидеры
- Модерн
- Trellis Bioscience
- SpyBiotech
- Викальный
- Atara Biotherapeutics
Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок - Конкурентное соперничество

Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
(Доминируют крупные игроки)
(Высококонкурентный с большим количеством игроков.)
Последние разработки в Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок
- В мае 2024 года в состав Moderna вошёл MRNA-1647. III фаза испытаний. Эта вакцина направлена на развитие иммунитета как к пентамеровому комплексу, так и к гликопротеину B ЦМВ, нацеленному на несколько путей, участвующих в инфекции ЦМВ.
- В апреле 2024 года Trellis Bioscience продолжила свою деятельность. Фаза Я исследовал TRL345, высокоаффинное человеческое антитело, которое нейтрализует ЦМВ, нацеливаясь на гликопротеин B, предотвращая вирусный проникновение в клетки человека.
- В марте 2024 года стартовал SpyBiotech Фаза Я проводил испытания SPYVLP01, кандидата на вакцину, использующего вирусоподобные частицы гепатита В для стимуляции иммунного ответа против ЦМВ, с целью предотвращения врожденного ЦМВ и других тяжелых инфекций у пациентов с ослабленным иммунитетом.
Цитомегаловирус (ЦМВ) Инфекционный терапевтический рынок Сегментация
- Тип препарата
- Вальгнцикловир
- Ганцикловир
- Сидофовир
- Фоскарнет
- С помощью приложения
- Трансплантация органов
- Трансплантация стволовых клеток
- Врожденный CMV инфекция
- Дистрибьюторский канал
- Больничные аптеки
- Розничные аптеки
- Онлайн аптеки

Хотите изучить возможность покупкиотдельные разделы этого отчета?
Часто задаваемые вопросы :
Насколько велик рынок терапевтической инфекции цитомегаловируса (ЦМВ)?
Глобальный рынок терапевтической терапии цитомегаловируса (ЦМВ) оценивается в 231,4 доллара США. Mn в 2024 году и, как ожидается, достигнет 370,2 млн долларов США к 2031 году.
Каким будет CAGR инфекционного терапевтического рынка цитомегаловируса (ЦМВ)?
Прогнозируется, что CAGR рынка инфекционной терапии цитомегаловируса (CMV) составит 7,10% с 2024 по 2031 год.
Каковы основные факторы, влияющие на рост рынка терапевтической терапии цитомегаловируса (ЦМВ)?
Растущее число пациентов с ослабленным иммунитетом, таких как те, кто получает трансплантацию органов, или те, кто живет с ВИЧ / СПИДом, стимулирует спрос на более эффективные методы лечения и профилактические вакцины для ЦМВ. Технологические достижения в разработке вакцин, особенно платформы на основе мРНК, способствуют созданию более эффективных вакцин, таких как мРНК-1647 от Moderna, которая нацелена как на пентамеровый комплекс, так и на гБ-белок для предотвращения инфекции ЦМВ, являются основным фактором, стимулирующим рынок терапевтической инфекции цитомегаловируса (ЦМВ).
Каковы ключевые факторы, препятствующие росту рынка терапевтической терапии цитомегаловируса (ЦМВ)?
Высокие затраты, связанные с передовым противовирусным лечением и вакцинами, могут ограничить доступ к эффективным методам лечения для пациентов в регионах с низким и средним уровнем дохода и лекарственной устойчивостью к доступным в настоящее время противовирусным препаратам, таким как Ганцикловир и Фоскарнет, усложняет лечение инфекции ЦМВ у пациентов с ослабленным иммунитетом, увеличивая потребность в новых терапевтических подходах, что является основным фактором, препятствующим росту рынка терапии инфекции Цитомегаловируса (ЦМВ).
Что является ведущим типом лекарств на терапевтическом рынке цитомегаловируса (ЦМВ)?
Valgnciclovir является ведущим сегментом лекарственных препаратов.
Каковы основные игроки, работающие на терапевтическом рынке инфекций цитомегаловируса (ЦМВ)?
Moderna, Trellis Bioscience, SpyBiotech, Vical, Atara Biotherapeutics, Chimerix Inc, Pfizer Inc, Merck & Company, Johnson & Johson, Bio-Rad Laboratories Inc, F.Hoffman La-Roche Ltd являются основными игроками.