Метастатический тройной негативный рак молочной железы (mTNBC) АНАЛИЗ РАЗМЕРОВ И ДОЛЕЙ - ТЕНДЕНЦИИ РОСТА И ПРОГНОЗЫ (2024 - 2031)
Метастатический тройной негативный рак молочной железы (mTNBC) Рынок сегментируется по терапии (химиотерапия, иммунотерапия, целевая терапия, новые ка....
Метастатический тройной негативный рак молочной железы (mTNBC) Размер
Размер рынка в долларах США Bn
CAGR5%
| Период исследования | 2024 - 2031 |
| Базовый год оценки | 2023 |
| CAGR | 5% |
| Концентрация рынка | Medium |
| Основные игроки | G1 Терапевтика, Фармабцин/Мерк, Roche/Genentech, Бристол Майерс Сквибб, АстраЗенека и среди других |
дайте нам знать!
Метастатический тройной негативный рак молочной железы (mTNBC) Анализ
Рынок метастатического тройного отрицательного рака молочной железы (mTNBC) оценивается как $1,57 млрд в 2024 году Ожидается, что он достигнет 2,2 млрд долларов к 2031 году, Растущий со сложным годовым темпом роста (CAGR) 5% с 2024 по 2031 год. Растущая заболеваемость раком молочной железы во всем мире и ограниченные варианты лечения мТНБК являются основными факторами, способствующими росту этого рынка.
Метастатический тройной негативный рак молочной железы (mTNBC) Тенденции
Рыночный драйвер - Новые иммуно-таргетинговые методы лечения, такие как ингибиторы контрольных точек, улучшают показатели выживаемости пациентов
Ингибиторы контрольных точек стали многообещающей стратегией лечения мТНБК в последние годы. Один класс ингибиторов контрольных точек, известный как ингибиторы PD-1 / PD-L1, показал особенно обнадеживающие результаты в клинических испытаниях для пациентов с мТНБК. Препараты, такие как атезолизумаб, авелумаб и дурвалумаб, блокируют путь PD-1 / PD-L1, который обычно используется раковыми заболеваниями для уклонения от обнаружения иммунной системы. Первоначальные исследования показали, что эти агенты могут достигать скорости ответа около 5-10% в качестве монотерапии в сильно обработанном мТНБК. Однако более поздние комбинированные испытания, сочетающие их с химиотерапией, показали, что частота ответов возрастает еще выше.
Возможно, наиболее важно то, что в настоящее время появляются данные о долгосрочной выживаемости, указывающие на то, что эти иммунные схемы могут значительно увеличить продолжительность жизни по сравнению с одной только химиотерапией. Поскольку ингибиторы контрольных точек продолжают демонстрировать устойчивые реакции и преимущества для выживания у более крупных и более длинных когорт пациентов с mTNBC, онкологи ожидают включения этих методов лечения в стандарты ухода.
Их новый механизм представляет собой потенциально важное достижение для этого исторически трудно поддающегося лечению рака. Широкое внедрение схем иммунного таргетирования может оказать глубокое влияние на результаты и дать надежду тем, кто сталкивается с этим агрессивным заболеванием.
Рыночный драйвер: повышение внимания к персонализированной медицине и целевой терапии
Одним из клинически важных подтипов являются опухоли с мутациями в гене BRCA1, на которые приходится около 10-15% всех случаев mTNBC. Раки с мутациями BRCA1, как правило, имеют различные биологические особенности и реакции на лечение по сравнению с другими mTNBC.
Это признание вызвало растущий интерес к разработке целевых методов лечения, адаптированных к конкретным молекулярным изменениям. Для BRCA1 мутировавшего mTNBC особенно перспективным классом являются ингибиторы PARP. Эти агенты блокируют путь восстановления ДНК, на который раковые клетки с мутациями BRCA1/2 полагаются для исправления повреждений, выталкивая их в клеточный кризис. Ранние исследования показали, что ингибиторы PARP, такие как талазопариб и олапариб, могут достигать объективных показателей ответа более 50% у BRCA1/2 мутировавшего mTNBC, предварительно обработанного химиотерапией, что гораздо более эффективно, чем у непревзойденных групп пациентов.
В результате производители лекарств проводят крупные регистрационные испытания ингибиторов PARP, специально регистрируя только случаи мутантного mTNBC BRCA1/2. Исследователи также изучают комбинации ингибиторов PARP, такие как платиновая химиотерапия или иммунотерапия, чтобы потенциально увеличить пользу. В целом, способность идентифицировать статус BRCA1 и нацеливать ингибирование PARP исключительно на эту генетическую подгруппу высокого риска дает новый оптимизм для улучшения результатов mTNBC с помощью индивидуальных подходов к медицине.

Новые методы лечения, особенно биологические препараты и генные методы лечения, остаются дорогостоящими, ограничивая доступность
Новые методы лечения, особенно биопрепараты и генные методы лечения метастатического тройного негативного рака молочной железы (mTNBC), остаются дорогостоящими, ограничивая их доступность для многих пациентов, которые в них нуждаются. Разработка новых биологических препаратов является дорогостоящей задачей, часто требующей миллиардов долларов финансирования исследований.
Выведение нового препарата на рынок также включает тщательное клиническое тестирование для подтверждения эффективности и безопасности. Эти обширные затраты на исследования и разработки, связанные с новыми лекарствами, в конечном итоге передаются потребителям в виде высоких цен. Например, недавние одобрения иммунотерапевтических препаратов, таких как пембролизумаб и атезолизумаб, для лечения mTNBC стоят более 10 000 долларов в месяц.
Кроме того, новые целевые методы лечения и генная терапия, которые показывают перспективы в клинических испытаниях, вероятно, будут иметь еще более высокие затраты, если они будут одобрены. Хотя эти новые методы лечения обеспечивают значительные клинические преимущества для mTNBC с небольшим количеством существующих вариантов лечения, барьер доступности не позволяет многим пациентам получить к ним доступ. Высокие расходы из своего кармана особенно влияют на незастрахованных или незастрахованных. Это оставляет значительную неудовлетворенную потребность в более экономически эффективных вариантах лечения мТНБК.
Рыночная возможность - растущие клинические испытания комбинированной терапии
Растет число исследований, оценивающих комбинированные схемы метастатического тройного негативного рака молочной железы (mTNBC), которые демонстрируют синергетическую противоопухолевую активность. Объединение существующих методов лечения, которые нацелены на различные пути, может улучшить клинические результаты по сравнению с одноагентными методами лечения.
Тем не менее, тщательно разработанные клинические испытания по-прежнему необходимы для установления безопасности, эффективности и оптимального секвенирования или планирования комбинированных схем. Все большее число фармацевтических компаний и академических исследовательских групп проводят испытания на соответствие концепции, сочетая иммунотерапию, химиотерапевтические агенты, таргетную терапию и другие новые классы лекарств.
Цель состоит в том, чтобы определить хорошо переносимые комбинированные стратегии, которые дают устойчивые ответы у пациентов с этим агрессивным подтипом заболевания. Положительные результаты текущих и запланированных испытаний комбинированной терапии могут установить новый стандарт протоколов лечения для mTNBC. Это дает возможность значительно продвинуться в лечении этого смертельного заболевания.
Предпочтения врачей Метастатический тройной негативный рак молочной железы (mTNBC)
Для лечения метастатического тройного отрицательного рака молочной железы первой линии, врачи обычно предпочитают схемы химиотерапии, такие как доцетаксел плюс карбоплатин или паклитаксел плюс карбоплатрим. Они используются, когда опухоль является гормон-рецептором отрицательным, а рецептор эпидермального фактора роста человека 2 (HER2) отрицательным.
Если рак прогрессирует после химиотерапии первой линии, варианты второй линии включают одноагентные химиотерапевтические препараты, такие как альдоксорубицин (IXEMPRA), мезилат эрибулина (Halaven) или гемцитабин (Gemzar). Иммунотерапевтические препараты, такие как атезолизумаб (Тецентрик) в сочетании с наб-паклитакселом (Абраксан), также получают признание в этой обстановке.
Для тех, кто получил два или более предыдущих методов лечения, исключая антрациклины и таксаны, ингибитор PARP олапариб (Lynparza) продемонстрировал эффективность и теперь является стандартным вариантом лечения третьей линии. Однако не все пациенты положительно относятся к мутациям BRCA зародышевой линии, которые предсказывают реакцию на ингибиторы PARP.
Помимо третьей линии, врачи прибегают к клиническим испытаниям исследуемых препаратов или лучшей поддерживающей терапии. Такие факторы, как статус производительности, функция органов, профиль мутации и предыдущие методы лечения, влияют на эти более поздние варианты. Агрессивные опухоли с быстрым рецидивом могут исключать дальнейшую химиотерапию, направляя назначенных пациентов на раннюю фазу испытаний, когда это возможно.
Анализ вариантов лечения Метастатический тройной негативный рак молочной железы (mTNBC)
mTNBC можно разделить на ранние или продвинутые стадии на основе размера опухоли, вовлечения узла и метастазирования. Лечение раннего mTNBC включает химиотерапию с последующей операцией. При прогрессирующем или метастатическом заболевании химиотерапия остается вариантом первой линии.
Стандартное лечение первой линии представляет собой химиотерапию на основе платины с использованием препаратов, таких как карбоплатин или цисплатин, в сочетании с другими агентами, такими как гемцитабин, паклитаксел или наб-паклитаксел. Обоснование заключается в том, что соли платины работают лучше для мТНБК из-за повышенной чувствительности к повреждению ДНК. Эти схемы обеспечивают объективную частоту ответа 30-50% и среднюю выживаемость без прогрессирования 6-8 месяцев.
Для тех, кто прогрессирует на платиновой терапии первой линии или не рассматривается по таким причинам, как почечная дисфункция, предпочтительным вариантом второй линии является монотерапия таксанами, такими как паклитаксел или наб-паклитаксел. Частота ответов составляет около 10-20% при ПФС 4-6 месяцев.
Для более поздних линий лечения при дальнейшем прогрессировании заболевания варианты химиотерапии включают эрибулин, винорелбин или капецитабин, хотя ответы ниже. Клинические испытания новой иммунотерапии и целевых препаратов также являются вариантами, где это возможно. Оптимальный выбор лечения взвешивает преимущества, токсичность и предпочтения пациента на каждой стадии заболевания, чтобы максимизировать время без прогрессирования.
Ключевые выигрышные стратегии, принятые ключевыми игроками Метастатический тройной негативный рак молочной железы (mTNBC)
Стратегическое сотрудничество и партнерство:
В 2021 году AstraZeneca вступила в клиническое сотрудничество с Daiichi Sankyo для оценки комбинации ENHERTU (fam-trastuzumab deruxtecan-nxki) и datopotamab deruxtecan у пациентов с mTNBC. Это партнерство позволит компаниям использовать свой опыт и ресурсы для ускорения разработки новых вариантов лечения.
В 2018 году Tesaro (в настоящее время входит в GSK) заключила партнерство с Debiopharm для коммерциализации нирапариба (Zejula) для пациентов с mTNBC в Европе. Это сотрудничество позволило обеим компаниям объединить свои коммерческие возможности и установить нирапариб в качестве важного варианта лечения в этой популяции пациентов.
Целевые приобретения:
В 2019 году Johnson & Johnson приобрела Janssen Biotech за $7,2 млрд, получив доступ к своему ингибитору PD-L1 бальстилимаб, который оценивается в сочетании с химиотерапией для mTNBC.
В 2018 году AstraZeneca приобрела MedImmune за 15 миллиардов долларов, добавив в свой трубопровод мирветуксимаб соравтанзин. Этот альфа-таргетированный антитело-лекарственный конъюгат с фолиевым рецептором находится на поздней стадии тестирования для mTNBC и имеет потенциал продаж блокбастеров, если он одобрен.
Надежные программы клинических испытаний:
В 2021 году GlaxoSmithKline сообщила о положительных результатах исследования фазы 3 PRIMARY, в котором Zejula оценивалась как адъювантная терапия для пациентов с mTNBC. В случае одобрения это может значительно расширить адресный рынок Zejula.
Сегментарный анализ Метастатический тройной негативный рак молочной железы (mTNBC)
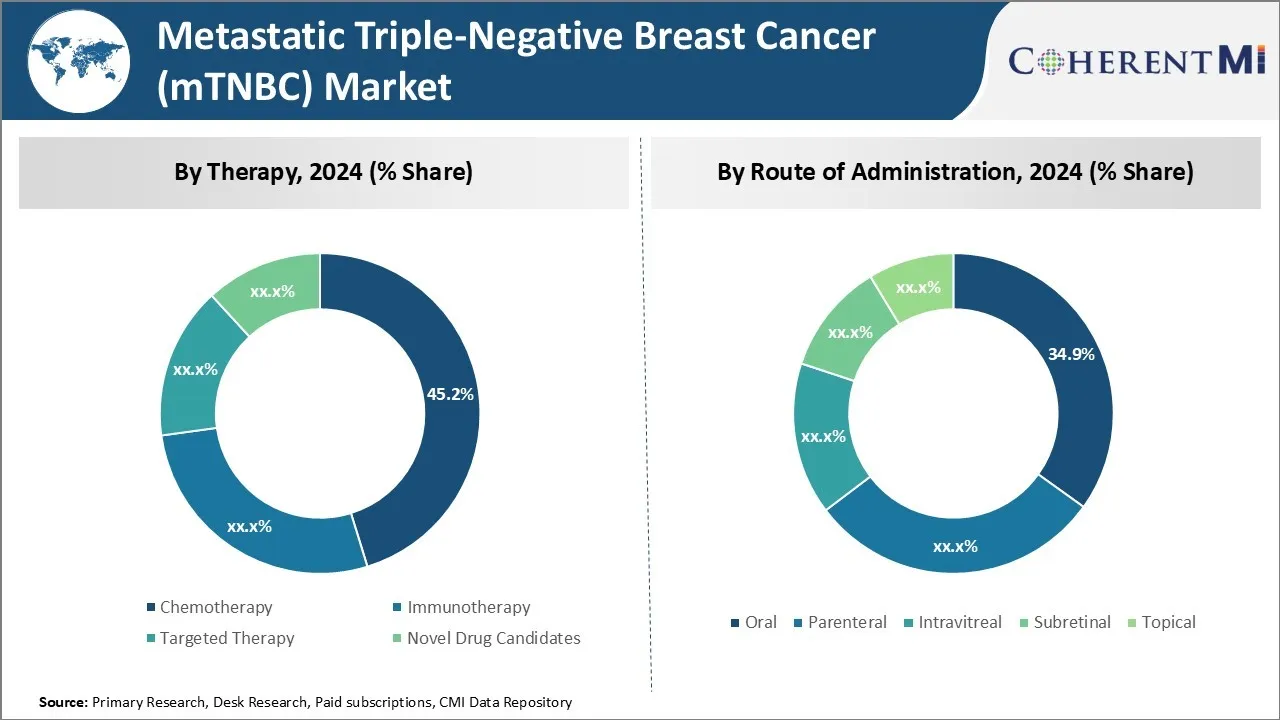
Проницательность: химиотерапия остается краеугольным камнем лечения mTNBC из-за ограниченных целевых альтернатив
По прогнозам, в 2024 году доля химиотерапии на рынке составит 45,2% из-за ограниченных эффективных целевых и иммунотерапевтических альтернатив для лечения мТНБК. Химиотерапия работает путем остановки или замедления роста раковых клеток, которые быстро растут и делятся. Многие типы химиотерапевтических препаратов вводятся вместе в циклах, чтобы иметь синергетический эффект при лечении мТНБК.
Некоторые распространенные химиотерапевтические препараты используются антрациклины, такие как доксорубицин, которые повреждают ДНК и таксаны, такие как паклитаксел и доцетаксел, которые мешают делению клеток. Хотя химиотерапия по-прежнему является важной частью лечения mTNBC, она также связана с токсическими побочными эффектами, которые влияют на качество жизни. Продолжаются исследовательские усилия по разработке новых целевых методов лечения и иммунотерапии с лучшими профилями эффективности и безопасности для замены химиотерапии в качестве лечения первой линии для mTNBC.
По пути администрирования: оральная терапия набирает обороты в качестве предпочтительного пути администрирования
Ожидается, что в 2024 году доля пероральной терапии на рынке составит 34,9% из-за предпочтения пациентов пероральным препаратам по сравнению с внутривенной терапией, требующей посещения больницы. Пероральный маршрут обеспечивает удобство с самоуправлением в домашних условиях, избегая воздействия больничных условий во время иммунодефицитных периодов. Это позволяет гибкие графики дозирования и улучшает соблюдение режима лечения.
Оральная терапия также помогает снизить расходы на здравоохранение за счет снижения административных сборов и расходов на пребывание в больнице. Фармацевтические компании разрабатывают новые ингибиторы малых молекул и моноклональные антитела с пероральными составами, чтобы извлечь выгоду из этой тенденции. Тем не менее, парентеральное введение по-прежнему доминирует в настоящее время из-за ограниченного количества эффективных пероральных альтернатив, доступных для лечения мТНБК.
Insights, By Distribution Channel: Госпитали доминируют в распределении, управляемом комплексной специальностью Потребности в уходе
С точки зрения канала дистрибуции больницам принадлежит наибольшая доля рынка, так как пациенты мТНБК нуждаются в комплексной междисциплинарной помощи с привлечением медицинских онкологов, радиационных онкологов, хирургов и других специалистов. Больницы оснащены специализированными онкологическими центрами, предлагающими комплексные услуги от диагностики до лечения и последующего ухода. Они также обеспечивают стационарное введение химиотерапии, лучевую терапию, хирургические сьюты и интенсивную терапию в случае осложнений, связанных с лечением, или неотложных медицинских ситуаций.
Учитывая агрессивный характер и ограниченные возможности лечения, пациенты предпочитают получать консультации экспертов и координированный уход в больницах, расположенных рядом с их домами. Специализированные клиники и онлайн-аптеки остаются нишевыми каналами распространения, поскольку более специализированная инфраструктура и опыт по-прежнему сосредоточены вокруг больниц для управления mTNBC.
Дополнительные идеи Метастатический тройной негативный рак молочной железы (mTNBC)
- 10-15% случаев рака молочной железы: Метастатический тройной негативный рак молочной железы представляет собой 10-15% всех случаев рака молочной железы, подчеркивая необходимость новых методов лечения для решения этой агрессивной формы.
- Проблемы лечения: быстрое распространение mTNBC и устойчивость к традиционным методам лечения подчеркивают актуальность клинических достижений.
- Трилацилиб от G1 Therapeutics: Значительное исследование III фазы для mTNBC, направленное на защиту от повреждения иммунной системы химиотерапией.
- Olinvacimab by PharmAbcine/Merck: Фаза II клинических испытаний в качестве антиангиогенного антитела, которое показало перспективность в ингибировании метастазирования в mTNBC.
- Сфокусируйтесь на биомаркерах: Усиливаются исследования по выявлению биомаркеров и генетических профилей для обеспечения персонализированных подходов к лечению, которые могут значительно улучшить результаты лечения пациентов.
Обзор конкурентов Метастатический тройной негативный рак молочной железы (mTNBC)
Основные игроки, работающие на рынке метастатического тройного отрицательного рака молочной железы (mTNBC), включают G1 Therapeutics, PharmAbcine / Merck, Roche / Genentech, Bristol Myers Squibb, AstraZeneca, Merck & Co., Gilead Sciences, Pfizer Inc., Novartis AG и Eli Lilly and Company.
Метастатический тройной негативный рак молочной железы (mTNBC) Лидеры
- G1 Терапевтика
- Фармабцин/Мерк
- Roche/Genentech
- Бристол Майерс Сквибб
- АстраЗенека
Метастатический тройной негативный рак молочной железы (mTNBC) - Конкурентное соперничество

Метастатический тройной негативный рак молочной железы (mTNBC)
(Доминируют крупные игроки)
(Высококонкурентный с большим количеством игроков.)
Последние разработки в Метастатический тройной негативный рак молочной железы (mTNBC)
- В июне 2024 года G1 Therapeutics объявила, что Трилациклиб, ингибитор CDK4/6, вступил в III фазу клинических испытаний для mTNBC. Эта терапия обеспечивает защиту костного мозга и усиливает долгосрочное иммунное наблюдение. Это развитие может значительно повлиять на выживаемость пациентов. Это исследование фокусируется на использовании трилацилиба, ингибитора CDK4/6, для защиты костного мозга и улучшения функции иммунной системы во время химиотерапии. В частности, его назначают перед химиотерапией (гемцитабин и карбоплатин) для уменьшения повреждающего воздействия цитотоксических методов лечения. Цель состоит в том, чтобы не только сохранить здоровье костного мозга, но и улучшить долгосрочное иммунное наблюдение.
- В декабре 2021 года PharmAbcine/Merck объявила, что Olinvacimab, антиангиогенное антитело, вступило в испытание фазы IIa в сочетании с Pembrolizumab для mTNBC. Его механизм нацелен на пути VEGF для ингибирования ангиогенеза опухоли, предлагая потенциал для повышения эффективности лечения. Испытание было начато на основе многообещающих ранних результатов исследования фазы Ib, которые показали обнадеживающую эффективность и хороший профиль безопасности. Испытание фазы II началось с целью оценки эффективности комбинации в ингибировании ангиогенеза опухоли через путь VEGFR2, на который нацелен Olinvacimab. Этот путь имеет решающее значение в блокировании образования кровеносных сосудов, которые опухоли нуждаются в росте и распространении.
- В июле 2021 года FDA предоставило ускоренное одобрение Keytruda в сочетании с химиотерапией для TNBC на ранней стадии высокого риска, расширяя его терапевтическое использование и предлагая надежду на лучшие результаты для пациентов. Это одобрение позволяет использовать Keytruda в качестве неоадъювантного лечения (до операции) в сочетании с химиотерапией и в качестве одноагентного адъювантного лечения. Это одобрение ознаменовало значительный шаг вперед в лечении TNBC, предлагая новый вариант иммунотерапии, который улучшил результаты у пациентов с ранней стадией TNBC высокого риска на основе результатов клинического исследования KEYNOTE-522.
- В ноябре 2020 года Merck & Co. сообщила о положительных результатах III фаза исследования KEYNOTE-355, в котором оценивали Keytruda (пембролизумаб) в сочетании с химиотерапией для лечения метастатического тройного негативного рака молочной железы (mTNBC). Исследование показало, что комбинация значительно улучшила выживаемость без прогрессирования (PFS) по сравнению с химиотерапией у пациентов, у которых опухоли экспрессировали PD-L1. Это стало важным достижением для лечения mTNBC, предлагая пациентам новый терапевтический вариант, в котором ранее были доступны ограниченные методы лечения.
- В апреле 2020 года FDA предоставило ускоренное одобрение Trodelvy (sacituzumab govitecan-hziy), разработанному Immunomedics, в настоящее время принадлежащему Gilead Sciences. Это одобрение было специально для взрослых пациентов с метастатическим тройным негативным раком молочной железы (mTNBC), которые ранее проходили по крайней мере две предыдущие терапии метастатического заболевания. Одобрение предоставило важный новый вариант лечения для пациентов с ограниченными альтернативами, особенно в тех случаях, когда стандартная химиотерапия больше не была эффективной.
Метастатический тройной негативный рак молочной железы (mTNBC) Сегментация
- Терапия
- Химиотерапия
- Антрациклины
- Таксаны
- Антиметаболиты
- Иммунотерапия
- Иммунные ингибиторы контрольных точек
- Раковые вакцины
- Таргетная терапия
- Ингибиторы PARP
- Конъюгаты антитело-наркотик
- Новые кандидаты на наркотики
- Химиотерапия
- По маршруту администрации
- устный
- родительский
- внутривитреальный
- Субретинальный
- тематический
- Дистрибьюторский канал
- Больницы
- Специальные клиники
- Онлайн аптеки

Хотите изучить возможность покупкиотдельные разделы этого отчета?
Часто задаваемые вопросы :
Насколько велик рынок метастатического тройного отрицательного рака молочной железы?
Рынок метастатического тройного отрицательного рака молочной железы (mTNBC) оценивается в 1,57 млрд долларов США в 2024 году и, как ожидается, достигнет 2,2 млрд долларов США к 2031 году.
Каковы ключевые факторы, препятствующие росту рынка метастатического тройного отрицательного рака молочной железы (mTNBC)?
Новые методы лечения, особенно биологические и генные, остаются дорогостоящими, ограничивая доступность. Кроме того, устойчивость к стандартной химиотерапии и таргетной терапии является основным фактором, препятствующим росту рынка метастатического тройного негативного рака молочной железы (mTNBC).
Каковы основные факторы, влияющие на рост рынка метастатического тройного отрицательного рака молочной железы (mTNBC)?
Новые иммуно-таргетинговые методы лечения, такие как ингибиторы контрольных точек, улучшают показатели выживаемости пациентов и уделяют все больше внимания персонализированной медицине и таргетной терапии, особенно для подтипов, таких как мутировавший mTNBC brca1, являются основными факторами, влияющими на рынок метастатического тройного негативного рака молочной железы (mTNBC).
Что является ведущей терапией на рынке метастатического тройного отрицательного рака молочной железы (mTNBC)?
Ведущим сегментом терапии является химиотерапия.
Какие основные игроки работают на рынке метастатического тройного отрицательного рака молочной железы (mTNBC)?
G1 Therapeutics, PharmAbcine/Merck, Roche/Genentech, Bristol Myers Squibb, AstraZeneca, Merck & Co., Gilead Sciences, Pfizer Inc., Novartis AG и Eli Lilly and Company являются основными игроками.
Каким будет CAGR рынка метастатического тройного отрицательного рака молочной железы (mTNBC)?
Прогнозируется, что CAGR рынка метастатического тройного отрицательного рака молочной железы (mTNBC) составит 5% с 2024 по 31 год.