Рынок ингибиторов SARM1 АНАЛИЗ РАЗМЕРОВ И ДОЛЕЙ - ТЕНДЕНЦИИ РОСТА И ПРОГНОЗЫ (2024 - 2031)
Рынок ингибиторов SARM1 сегментирован по показаниям (амиотрофический боковой склероз, рассеянный склероз, периферические невропатии, глаукома) По типу....
Рынок ингибиторов SARM1 Размер
Размер рынка в долларах США Mn
CAGR103.7%
| Период исследования | 2024 - 2031 |
| Базовый год оценки | 2023 |
| CAGR | 103.7% |
| Концентрация рынка | Medium |
| Основные игроки | Разоружить терапевтические средства, Нура Био, Вашингтонский университет, Аша Терапевтика, UCB Фармацевтика и среди других |
дайте нам знать!
Рынок ингибиторов SARM1 Анализ
Ингибиторы SARM1 Рынок оценивается в 5 млн долларов в 2024 году Ожидается, что он достигнет 727 млн долларов США к 2031 году, растущие с совокупным годовым темпом роста (CAGR) 103,7% с 2024 по 2031 год.
Ожидается, что рынок будет наблюдать положительный рост в течение прогнозируемого периода. Ожидается, что такие факторы, как высокая распространенность неврологических расстройств, таких как травмы спинного мозга, и растущие исследования и разработки новых молекул лекарств будут стимулировать спрос. Перспективные результаты клинических испытаний ингибиторов SARM1 при лечении различных неврологических состояний дополнительно дадут толчок росту. Кроме того, ожидается, что рост гериатрического населения, склонного к неврологическим заболеваниям, в дополнение к увеличению расходов на здравоохранение будет поддерживать генерацию доходов.
Рынок ингибиторов SARM1 Тенденции
Рост инвестиций в неврологические исследования, особенно в ингибирование SARM1, стимулирует рынок.
За последние несколько лет инвестиции в неврологические исследования неуклонно росли. Растет признание воздействия нейродегенеративных заболеваний на общественное здравоохранение и экономику. Несколько финансирующих учреждений и фондов увеличили свои бюджеты на поиск лечения таких состояний, как болезнь Альцгеймера, болезнь Паркинсона и БАС. Исследования механизмов, лежащих в основе дегенерации аксона, получили значительную поддержку. Одной из перспективных новых областей является ингибирование SARM1.
Исследования показали, что SARM1 играет ключевую роль в самоуничтожении аксона, особенно после травмы. Блокирование SARM1 может предотвратить повреждение нервов от различных неврологических нарушений и заболеваний. Это вызвало огромный интерес как со стороны государственных, так и частных спонсоров. За последние пять лет гранты NIH, направленные на биологию SARM1 и ее терапевтический потенциал, удвоились. Несколько фармацевтических и биотехнологических компаний также вошли в эту область через приобретения и внутренние исследовательские инициативы. Некоторые из них продвинули ингибиторы-кандидаты в доклиническое и клиническое тестирование.
Рыночный драйвер - рост распространенности нейродегенеративных заболеваний во всем мире
Нейродегенеративные состояния, такие как болезнь Альцгеймера и Паркинсона, растут с угрожающей скоростью по мере старения населения во всем мире. По оценкам, в настоящее время более 50 миллионов человек во всем мире живут с деменцией, и ожидается, что в ближайшие десятилетия их число утроится. Даже в странах с улучшенными системами здравоохранения и ожидаемой продолжительностью жизни распространенность этих заболеваний продолжает неуклонно расти. Личное и социальное бремя нейродегенерации огромно и будет продолжать расти, если не появятся эффективные варианты лечения.
Пациенты и их опекуны отчаянно нуждаются в терапии, которая может замедлить или остановить прогрессирование заболевания. Отсутствие одобренных модифицирующих болезнь методов лечения оставило большую неудовлетворенную потребность. В последние годы многочисленные клинические испытания потенциальных методов лечения потерпели неудачу по различным причинам. Это повысило актуальность изучения новых путей и целей. Ингибирование SARM1 является многообещающим способом, поскольку оно может обеспечить нейропротекцию в широком спектре неврологических состояний. Блокирование пути SARM1 может оказаться скорее модифицирующим заболевание, чем симптоматическим. Значительные ресурсы направляются на проверку SARM1 в качестве лекарственной мишени для нейродегенерации.

Высокая стоимость и сложность разработки лекарств для нейродегенеративных расстройств могут ограничить рост рынка
Разработка лекарств для лечения нейродегенеративных расстройств создает значительные проблемы из-за сложного характера заболеваний и ограниченного понимания путей и механизмов заболевания. Открытие и разработка лекарств включает длительные клинические испытания, охватывающие несколько лет, для проверки эффективности и безопасности. Однако нейродегенеративные заболевания обычно затрагивают пожилых людей, которые могут не иметь права на клинические испытания из-за сопутствующих заболеваний. Кроме того, результаты могут быть трудно измерить объективно, и конечным точкам может потребоваться показать изменения в функционировании в течение многих лет. Эти факторы сложности способствуют высоким затратам на разработку, с оценками от 800 миллионов до 2 миллиардов долларов за каждый новый препарат. Производители должны учитывать восстановление затрат и балансирование высоких инвестиций в НИОКР с ценообразованием. Риск отказа от наркотиков остается высоким даже после крупных инвестиций. Эти рыночные барьеры могут лишить стимулов инвестиции в области редких заболеваний, таких как нейродегенерация. Высокие цены на лекарства также могут ограничить доступ пациентов. В целом, связанные с этим издержки и присущая им неопределенность создают значительные проблемы для роста рынка.
Возможности рынка: достижения в области точной медицины открывают новые возможности для роста
В последние годы наблюдается значительный прогресс в понимании генетического вклада и молекулярных путей, участвующих в нейродегенеративных расстройствах. Это позволило применять точные или персонализированные подходы к медицине, ориентированные на конкретные группы пациентов. Например, выявление биомаркеров, которые стратифицируют пациентов на основе подтипов заболевания или стадий прогрессирования, позволяет более четко оценить эффективность препарата. Достигнуты также успехи в разработке методов лечения с учетом генетических мутаций, связанных с семейными формами заболеваний. Эти персонализированные стратегии обещают более эффективно лечить подгруппы пациентов. Кроме того, новые технологии, такие как компьютерное моделирование сетей мозга, предлагают потенциал для лучшего прогнозирования эффектов лекарств и оптимизации режимов дозирования. Такие точные подходы направлены на максимизацию преимуществ и минимизацию побочных эффектов для пациентов. В случае успеха они могут оправдать более высокие цены на лекарства и способствовать дальнейшим инвестициям. В целом, продолжающийся прогресс в стратификации этих сложных заболеваний обеспечивает значительный потенциал роста для молекулярно-ориентированной терапии ингибиторами SARM1.
Предпочтения врачей Рынок ингибиторов SARM1
Лечение нейродегенеративных заболеваний обычно следует поэтапному подходу, основанному на прогрессировании заболевания и тяжести симптомов. Для легких случаев болезни Альцгеймера, назначающие обычно начинают с ингибиторов холинэстеразы, таких как донепезил (Aricept). Эти препараты работают, чтобы повысить уровень ацетилхолина в мозге и обеспечить когнитивные преимущества.
По мере того, как болезнь Альцгеймера переходит в умеренную стадию, может быть назначена комбинированная терапия для лечения нескольких симптомов. Общим режимом является донепезил плюс мемантин (Наменда), антагонист N-метил D-аспартатного рецептора. Эта комбинация препаратов направлена на улучшение памяти, мышления, поведения и повседневной функции.
Для поздней стадии болезни Альцгеймера и тяжелой деменции важны нефармакологические подходы. На данный момент лекарства дают мало когнитивной пользы, но могут помочь управлять поведением, таким как агрессия, беспокойство и бессонница. Антипсихотики, такие как кветиапин (сероквель), часто используются для их седативных эффектов.
Помимо лекарств, врачи также учитывают такие факторы, как страхование, стоимость для пациентов, поддержка по уходу и способность придерживаться графиков дозировки. На их предпочтения могут влиять данные клинических испытаний, а также взаимодействие с фармацевтическими представителями и лидерами мнений.
Анализ вариантов лечения Рынок ингибиторов SARM1
Рак легких обычно классифицируется на четыре основные стадии — I, II, III и IV — в зависимости от размера и распространения первичной опухоли и от того, метастазировал ли он в лимфатические узлы или отдаленные органы. Варианты лечения значительно варьируются в зависимости от стадии.
Для стадии I немелкоклеточного рака легких (NSCLC) предпочтительным вариантом обычно является операция по удалению опухоли. Для II стадии хирургия снова является основным выбором и может быть дополнена адъювантной химиотерапией с использованием дублета на основе платины, такого как цисплатин / карбоплатин, с такими препаратами, как пеметрекс, гемцитабин или таксаны, чтобы снизить риск рецидива. Стадия III NSCLC включает в себя вовлечение лимфатических узлов, что делает его менее подходящим для операции. Стандартом ухода является неоадъювантная химиотерапия с цисплатином / карбоплатином плюс таксан, за которой следует одновременное химиооблучение с использованием схемы на основе платины с лучевой терапией. За этим иногда следует адъювантная иммунотерапия такими препаратами, как пембролизумаб или ниволумаб, чтобы активировать иммунную систему против клеток рака легких.
Для метастатического NSCLC стадии IV, платиново-двойная химиотерапия остается вариантом первой линии. Тем не менее, иммунотерапия ингибиторами PD-1, такими как пембролизумаб, ниволумаб или атезолизумаб, становится все более заметным лечением первой линии из-за превосходной эффективности и снижения побочных эффектов по сравнению с химиотерапией. Для пациентов с мутациями EGFR или ALK предпочтительны целевые методы лечения, такие как гефитиниб, эрлотиниб или алектиниб.
Ключевые выигрышные стратегии, принятые ключевыми игроками Рынок ингибиторов SARM1
Сотрудничество и партнерские отношения были основной выигрышной стратегией для компаний в этой области. В 2021 году Cleave Therapeutics вступила в сотрудничество с Eli Lilly для разработки и коммерциализации ингибиторов SARM1 для дегенеративных заболеваний. Это дало Cleave доступ к значительным возможностям Lilly в области НИОКР и коммерциализации при одновременном снижении затрат на разработку.
Ориентация на индикаторы с высокой неудовлетворенной потребностью и рыночным потенциалом также оказалась успешной. В 2020 году Astellas решила разработать ингибитор SARM1 ASP-7037 для спинальной мышечной атрофии (SMA). SMA представляет собой огромную рыночную возможность, учитывая, что существует только два одобренных метода лечения. Ориентируясь на эту индикацию, Astellas позиционировала себя, чтобы захватить большую часть рынка SMA, если ASP-7037 будет одобрен.
Сосредоточение внимания на нейродегенеративных заболеваниях окупилось, поскольку они представляют собой большие группы пациентов, и возмещение часто является благоприятным. Расстройства, такие как БАС, РС и повреждение спинного мозга, имеют несколько одобренных вариантов лечения, поэтому ингибиторы SARM1 могут быстро внедряться. Клив и Астроцит специально разрабатывают методы лечения БАС и травмы спинного мозга на основе этой стратегии.
Быстрое продвижение клинических программ также помогло компаниям создать конкурентную позицию. Cleave инициировал испытание фазы 1 CLV-048 в течение 12 месяцев после основания и сообщил о первоначальных результатах за 18 месяцев, продемонстрировав скорость прогрессирования. Быстрое клиническое продвижение сигнализирует о приверженности и программах снижения риска от конкурирующих методов лечения.
Лицензирование одобренных технологий ускорило сроки разработки. В 2019 году Astellas лицензировала права на ASP-7037 от Astrocite, что позволило ей использовать доклинические работы, уже завершенные над соединением, и продвигать его в клинические испытания быстрее по сравнению с внутренним открытием. Это позволило Astellas установить преимущество раннего перехода в клинике по сравнению с внутренними трубопроводными программами.
Сегментарный анализ Рынок ингибиторов SARM1
Прозрения, по показаниям: Неудовлетворенные медицинские потребности способствуют росту рынка амиотрофического бокового склероза
Амиотрофический боковой склероз (БАС), также известный как болезнь Лу Герига, вносит наибольшую долю в 45,7% на рынке ингибиторов SARM1 из-за значительных неудовлетворенных медицинских потребностей. БАС является смертельным нейродегенеративным заболеванием с ограниченными вариантами лечения и высокими показателями смертности. В настоящее время нет лекарства от БАС, и единственный одобренный FDA препарат, Рилузол, обеспечивает скромные преимущества. Это ясно указывает на высокую неудовлетворенную потребность в более эффективных методах лечения.
Ингибирование SARM1 становится перспективным терапевтическим подходом для БАС. Доклинические исследования показали, что SARM1 играет важную роль в нейровоспалении и гибели нейронных клеток, связанных с БАС. Ингибирование SARM1 может потенциально остановить прогрессирование заболевания, предотвращая дегенерацию аксонов и потерю нейронов. Несколько фармацевтических компаний активно разрабатывают ингибиторы SARM1 для ALS с некоторыми кандидатами уже в клинических испытаниях. Если доказано, что эти ингибиторы безопасны и эффективны, они могут обеспечить значительные клинические преимущества для пациентов с БАС и даже стать стандартом лечения.
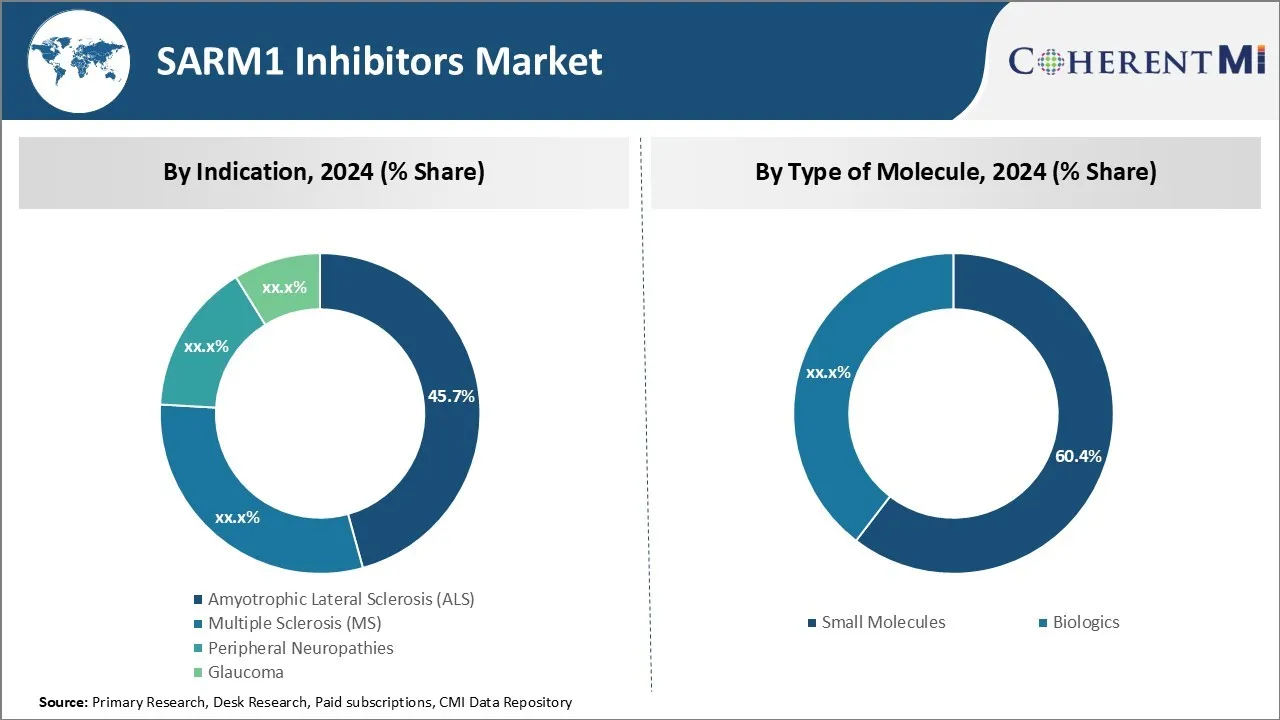
Прозрения, по типу молекул: Преимущества перед биологическими препаратами стимулируют спрос на небольшие молекулы
Подсегмент малых молекул доминирует на рынке ингибиторов SARM1 с долей рынка 60,4%, благодаря различным преимуществам перед биологическими молекулами. Малые молекулы легче разрабатывать и производить в больших масштабах по сравнению с биологическими препаратами. Они обладают лучшей стабильностью, требуют менее сложной цепочки поставок и контроля качества. Что еще более важно, небольшие молекулы обычно демонстрируют превосходное проникновение в ткани и достигают более высоких концентраций в центральной нервной системе (ЦНС).
Ориентация на SARM1, белок, локализованный в аксонах и телах нейронных клеток, требует ингибиторов с отличной способностью проникновения ЦНС. Большинство пациентов с БАС также имеют значительную нервно-мышечную денервацию, которая требует ингибиторов, которые могут эффективно достигать дегенеративных двигательных нейронов и нервно-мышечных соединений. Небольшие молекулы, благодаря своим оптимальным физико-химическим свойствам, лучше оснащены, чем биологические, для преодоления гематоэнцефалического барьера и достижения субклеточных участков действия SARM1. Эти критические фармакокинетические преимущества делают ингибиторы SARM1 очень желательными для разработки эффективных методов лечения БАС.
Дополнительные идеи Рынок ингибиторов SARM1
- Рынок ингибиторов SARM1 готов к экспоненциальному росту, что обусловлено ростом инвестиций в исследования, особенно в Северной Америке. Растущая распространенность нейродегенеративных заболеваний, таких как БАС и РС, в сочетании с достижениями в области точной медицины позиционирует ингибиторы SARM1 в качестве перспективного терапевтического рубежа. Быстрое расширение рынка также подпитывается продолжающимися доклиническими исследованиями и растущим участием как академических учреждений, так и биотехнологических компаний.
- Вашингтонский университет получил 64% грантов на исследования SARM1, что подчеркивает его ключевую роль в рыночных инновациях.
Обзор конкурентов Рынок ингибиторов SARM1
Основными игроками на рынке ингибиторов SARM1 являются Disarm Therapeutics, Nura Bio, Вашингтонский университет, Asha Therapeutics и UCB Pharma.
Рынок ингибиторов SARM1 Лидеры
- Разоружить терапевтические средства
- Нура Био
- Вашингтонский университет
- Аша Терапевтика
- UCB Фармацевтика
Рынок ингибиторов SARM1 - Конкурентное соперничество

Рынок ингибиторов SARM1
(Доминируют крупные игроки)
(Высококонкурентный с большим количеством игроков.)
Последние разработки в Рынок ингибиторов SARM1
- В апреле 2024 года Asha Therapeutics объявила о доклинических исследованиях ASHA-624, перспективной терапии, направленной на ингибирование белка SARM1 для лечения БАС, что указывает на потенциальное расширение рынка.
- В июне 2023 года Вашингтонский университет получил самые высокие гранты на исследования SARM1, укрепив свои лидирующие позиции на рынке.
Рынок ингибиторов SARM1 Сегментация
- По показаниям
- Амиотрофический боковой склероз (ALS)
- Множественный склероз (MS)
- Периферические невропатии
- глаукома
- По типу молекул
- Маленькие молекулы
- биологические

Хотите изучить возможность покупкиотдельные разделы этого отчета?
Часто задаваемые вопросы :
Каковы основные факторы, препятствующие росту рынка ингибиторов SARM1?
Высокая стоимость и сложность разработки лекарств для нейродегенеративных расстройств и проблемы регулирования в утверждении новых методов лечения нейродегенеративных состояний являются основными факторами, препятствующими росту рынка ингибиторов SARM1.
Каковы основные факторы, влияющие на рост рынка ингибиторов SARM1?
Увеличение инвестиций в неврологические исследования, особенно в ингибирование sarm1, и рост распространенности нейродегенеративных заболеваний во всем мире являются основными факторами, влияющими на рынок ингибиторов SARM1.
Что является ведущим индикатором на рынке ингибиторов SARM1?
Ведущим показанием сегмента является амиотрофический боковой склероз (ALS).
Какие основные игроки работают на рынке ингибиторов SARM1?
Disarm Therapeutics, Nura Bio, Вашингтонский университет, Asha Therapeutics и UCB Pharma являются основными игроками.
Каким будет CAGR на рынке ингибиторов SARM1?
Прогнозируется, что CAGR рынка ингибиторов SARM1 составит 103,7% с 2024 по 31 год.