Рынок перитонального рака АНАЛИЗ РАЗМЕРОВ И ДОЛЕЙ - ТЕНДЕНЦИИ РОСТА И ПРОГНОЗЫ (2024 - 2031)
Рынок перитонеального рака сегментирован По типу лекарств (продукты поздней стадии, продукты средней стадии, продукты ранней стадии), по маршруту адми....
Рынок перитонального рака Размер
Размер рынка в долларах США Bn
CAGR17.9%
| Период исследования | 2024 - 2031 |
| Базовый год оценки | 2023 |
| CAGR | 17.9% |
| Концентрация рынка | High |
| Основные игроки | AB Наука, Компания Zentalis Pharmaceuticals, Иммуноген, Юго-западный медицинский центр, Авастин и среди других |
дайте нам знать!
Рынок перитонального рака Анализ
Мировой рынок перитонеального рака оценивается как USD 5,9 млрд в 2024 году Ожидается, что он достигнет 15,9 долларов США Bn к 2031 году, Растущий со сложным годовым темпом роста (CAGR) 17,9% с 2024 по 2031 год.
Ожидается, что рынок будет наблюдать положительный рост в течение прогнозируемого периода. Ожидается, что рост заболеваемости карциноматозом брюшины из-за растущей распространенности таких видов рака, как рак яичников и желудка, будет стимулировать рынок. Кроме того, ожидается, что растущая осведомленность о вариантах диагностики и лечения перитонеального карциноматоза также повысит спрос. Кроме того, продолжающиеся клинические испытания, оценивающие эффективность нескольких системных методов лечения брюшинного карциноматоза, будут способствовать росту рынка. Однако высокие затраты, связанные с диагностикой и лечением, могут в некоторой степени препятствовать росту рынка. В целом, рост расходов на здравоохранение и спрос на передовые линии лечения рака брюшины во всем мире будут продолжать поддерживать расширение рынка в течение следующих нескольких лет.
Рынок перитонального рака Тенденции
Драйвер рынка - Достижения в области целевой терапии, включая ингибиторы PARP и целевые препараты, такие как Авастин, улучшают выживаемость пациентов и варианты лечения.
Целенаправленная терапия показала большие перспективы в улучшении результатов лечения для пациентов с раком брюшины. Такие препараты, как ингибиторы PARP и Авастин, которые предназначены для нацеливания на конкретные молекулярные пути, способствующие росту и распространению рака, получают признание в качестве стандартных вариантов лечения. Ингибиторы PARP, в частности, используют недостатки восстановления повреждений ДНК при раковых заболеваниях с мутациями BRCA и продемонстрировали способность значительно расширять без прогрессирования и общую выживаемость.
Несколько недавних клинических исследований подтвердили роль ингибиторов PARP, таких как олапариб и нирапариб, в рецидиве чувствительного к платине рака яичников. По сравнению с обычной химиотерапией добавление ингибитора PARP привело к тому, что средняя выживаемость без прогрессирования увеличилась почти до двух лет. В настоящее время исследователи изучают потенциал неоадъювантной терапии ингибиторами PARP, проводимой в рамках первоначального лечения до операции, чтобы лучше бороться с микроскопическим распространением рака. Авастин также доказал свою эффективность при добавлении к стандартной химиотерапии. Ингибируя VEGF, этот препарат от антител голодает опухоли кровоснабжения, необходимые для агрессивного роста. Его включение в протокол лечения рака яичников первой линии привело к улучшению результатов.
Накопление доказательств, подчеркивающих превосходство целевых схем лечения над традиционной химиотерапией, побуждает медицинские организации обновлять руководящие принципы лечения. Ингибиторы PARP, в частности, получают одобрение на более широкие сценарии использования на более поздней стадии, а также на ранних стадиях заболевания. Расширенный доступ к прецизионным лекарствам позволит большему количеству пациентов с раком брюшины получить более длительные ремиссии и надежду на управление своим заболеванием как хроническим заболеванием. Такие достижения улучшают качество жизни за счет снижения токсичных побочных эффектов, наблюдаемых только при химиотерапии. В целом, таргетная терапия является основным фактором расширения выбора лечения и увеличения выживаемости.
Рыночная возможность - Циторедуктивная хирургия в сочетании с HIPEC.
Появление циторедуктивной хирургии в сочетании с гипертермической внутрибрюшинной химиотерапией (HIPEC) в качестве потенциально лечебного варианта для некоторых злокачественных новообразований брюшинной поверхности изменило управление этими исторически трудными для лечения раковыми заболеваниями. В этой процедуре любые видимые опухолевые узелки хирургически удаляются из брюшной полости вместе с перитонэктомией, чтобы удалить микроскопические отложения болезни. Нагретая химиотерапия затем циркулирует в открытом животе, чтобы непосредственно купать поверхности брюшины и уничтожать любые оставшиеся раковые клетки.
Большие испытания III фазы продемонстрировали, что HIPEC в сочетании с оптимальной хирургией дебулкинга может более чем удвоить долгосрочные показатели выживаемости для пациентов с псевдомиксомой брюшины и колоректальным раком с изолированными метастазами брюшины по сравнению с одной только хирургией. Мета-анализ, объединяющий данные более чем 3000 пациентов с несколькими типами опухолей, показал, что процедура улучшает 5-летнюю выживаемость с примерно 15% при хирургическом вмешательстве до более 50%. Впечатляющие долгосрочные преимущества для выживания в течение более 20 лет наблюдались в некоторых подмножествах пациентов. Кроме того, лечение контролирует симптомы, удаляя опухоли, вызывающие растяжение живота и обструкцию.
Учитывая растущие доказательства, экспертные консенсусные группы теперь рекомендуют рассмотреть циторедуктивную хирургию с HIPEC для надлежащим образом выбранных пациентов с раком яичников III и IV стадии, аппендикса, колоректального рака и мезотелиомы. Многие крупные центры сообщили о низкой периоперационной заболеваемости и смертности менее 5% при выполнении опытными хирургическими онкологами. Несмотря на то, что этот агрессивный мультимодальный подход все еще экспериментальный для некоторых показаний, он предлагает потенциально лечебные результаты для рака брюшинной поверхности, который ранее считался неизлечимым.
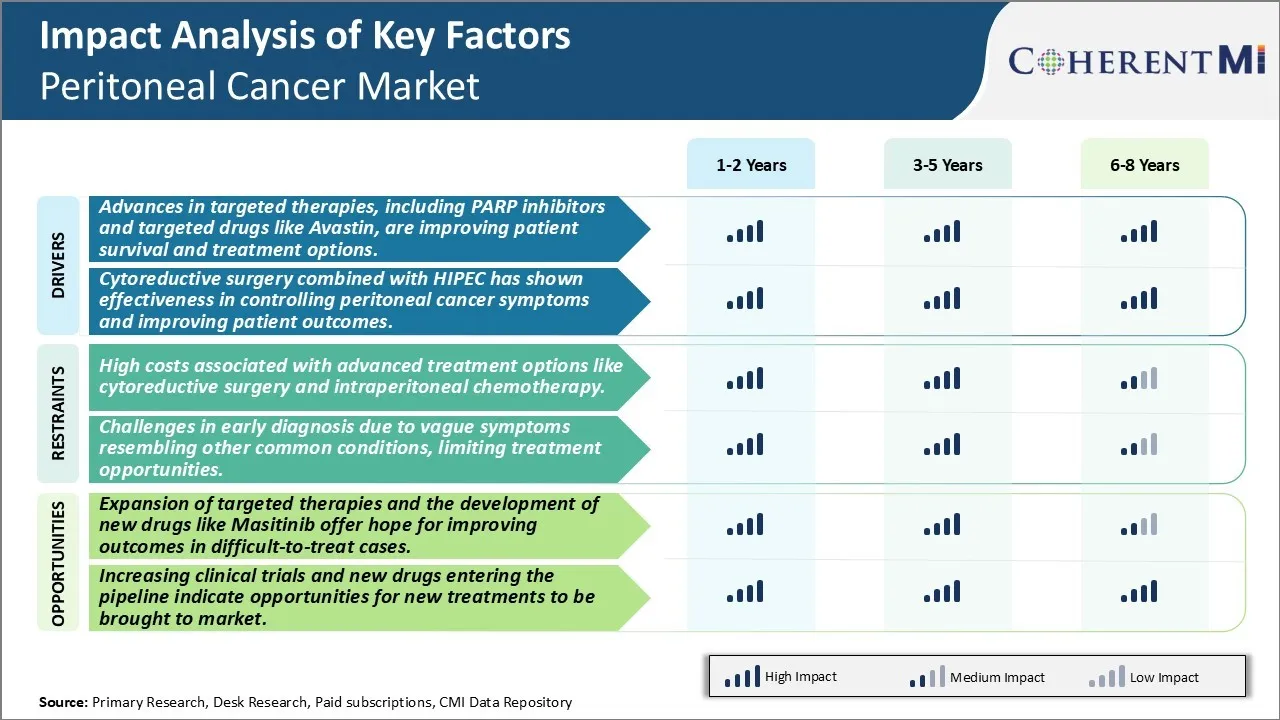
Вызов рынка - высокие затраты, связанные с расширенными вариантами лечения, такими как циторедуктивная хирургия и внутрибрюшинная химиотерапия.
Высокие затраты, связанные с расширенными вариантами лечения, такими как циторедуктивная хирургия и внутрибрюшинная химиотерапия.
Перитонеальный рак является относительно редкой, но агрессивной формой рака. Варианты лечения для пациентов с диагнозом более продвинутой стадии рака брюшины обычно включают сложные мультимодальные подходы, сочетающие хирургическое удаление всех видимых опухолей с помощью циторедуктивной хирургии с последующей внутрибрюшинной химиотерапией, доставляемой непосредственно в брюшную полость. Однако эти комплексные схемы лечения сопряжены со значительными расходами. Циторедуктивная хирургия является длительной и технически сложной процедурой, которая требует высококвалифицированных хирургов. Он также несет риски хирургических осложнений. Аналогичным образом, внутрибрюшинная химиотерапия требует размещения катетеров в брюшной полости, что является специализированной процедурой. Лекарственные препараты также имеют высокие цены. Все эти факторы способствуют тому, что эти передовые подходы к лечению стоят непомерно дорого для многих систем здравоохранения и пациентов. Высокие затраты часто служат барьером, ограничивающим доступ к потенциально лечебной мультимодальной терапии, особенно в небольших центрах и на развивающихся рынках. Это остается серьезной проблемой для более широкого принятия и улучшения результатов при раке брюшины.
Расширение целевой терапии и разработка новых лекарств, таких как Маситиниб, дают надежду на улучшение результатов в случаях трудного лечения.
Перспективный путь для лучшего управления раком брюшины включает в себя разработку целевых методов лечения и иммунотерапии. Несколько фармацевтических компаний имеют в клинических испытаниях препараты-кандидаты, которые направлены на блокирование определенных путей, способствующих росту рака или стимулирующих иммунную систему атаковать опухолевые клетки. Например, Masitinib является исследуемым пероральным ингибитором тирозинкиназы, который изучается для потенциального использования в рефрактерных случаях метастатического рака брюшины. Предварительные исследования показывают, что Маситиниб может увеличить без прогрессирования и общую выживаемость в селективных подгруппах пациентов. Его пероральное введение также предлагает преимущества перед инфузионными препаратами с точки зрения удобства и экономии средств. Поскольку исследования дают новые терапевтические возможности с более доступными и управляемыми подходами к введению, возможности будут расти, чтобы улучшить результаты даже у пациентов, которые не могут проходить интенсивное хирургическое лечение или которые испытывают рецидив заболевания. Это может значительно увеличить объем рынка в долгосрочной перспективе.
Предпочтения врачей Рынок перитонального рака
Перитонеальный рак обычно лечится на основе стадии прогрессирования заболевания. На ранних стадиях (I-II) операция по удалению видимых опухолей является основной линией лечения. В более сложных случаях химиотерапия часто назначается до или после операции.
На более поздних стадиях (III-IV) первая линия химиотерапии обычно включает режим на основе платины. Карбоплатин (параплатин) в сочетании с паклитакселом (таксол) обычно назначают из-за его эффективности. Для пациентов, которые не переносят платиновые препараты или тех, кто испытывает прогрессирование заболевания при лечении первой линии, режим второй линии может включать доксил (инъекция доксорубицина HCL-липосомы) или гемзар (гемцитабин HCl).
Для рецидивирующих или рефрактерных заболеваний новые целевые методы лечения стали вариантами третьей линии. Lartruvo (оларатумаб) в сочетании с доксилом показал улучшение выживаемости без прогрессирования и часто назначается. Другой перспективной альтернативой является Stivarga (regorafenib), ингибитор мультикиназы, который продемонстрировал общую пользу для выживания по сравнению с лучшим вспомогательным лечением.
Ключевые факторы, влияющие на предпочтения назначающих, включают эффективность препарата на основе последних клинических испытаний, профиль токсичности, страховое покрытие, стоимость лечения и сопутствующие заболевания / соответствие пациентов. Хирургия не всегда возможна в зависимости от степени заболевания, и толерантность к различным схемам химиотерапии также играет роль в выборе линии.
Анализ вариантов лечения Рынок перитонального рака
Перитонеальный рак диагностируется на четырех основных стадиях - от стадии I до стадии IV - в зависимости от того, насколько рак распространился. Лечение зависит от стадии рака и общего состояния здоровья пациента.
Для стадии I / II заболевания первичным лечением является циторедуктивная хирургия (CRS), процедура удаления видимых опухолей из брюшины. Это часто сочетается с гипертермической внутрибрюшинной химиотерапией (HIPEC), где химиотерапевтический препарат, такой как цисплатин, нагревается и циркулирует по всей брюшинной полости во время операции. HIPEC стремится уничтожить оставшиеся раковые клетки. Для III/IV стадии болезни, которая широко распространилась, CRS+HIPEC все еще может быть предпринята попытка, но имеет меньше шансов на излечение.
Если CRS+HIPEC невозможен, системная химиотерапия с использованием комбинаций, таких как карбоплатин плюс паклитаксел, является основным методом лечения. Это вводится внутривенно и путешествует по всему телу, чтобы нацелиться на раковые клетки. Для рецидивирующего заболевания после первоначального лечения варианты второй линии включают схемы с такими препаратами, как оксалиплатин или иринотекан, либо отдельно, либо с 5-FU. Также могут быть рассмотрены клинические испытания новых целевых терапий или иммунотерапевтических препаратов.
В заключение, CRS+HIPEC обеспечивает наилучшие шансы на излечение от ранней стадии заболевания из-за прямого контакта химиотерапевтического агента с опухолевыми участками. Для продвинутых или рецидивирующих стадий, когда операция невозможна, внутривенная химиотерапия направлена на продление жизни путем замедления прогрессирования заболевания.
Ключевые выигрышные стратегии, принятые ключевыми игроками Рынок перитонального рака
Ориентация на целевую разработку лекарств: Такие компании, как Eisai Co. и Merck & Co., сосредоточили свои усилия в области исследований и разработок на разработке целевых методов лечения рака брюшины. Эйсаи разработал Халавен (эрибулин), антимикротрубочный агент, показанный для метастатического рака молочной железы. В исследовании фазы 3, завершенном в 2011 году, Халавен показал улучшение общей выживаемости по сравнению с лечением выбора врача у женщин с прогрессирующей липосаркомой или лейомиосаркомой. Merck разработала Keytruda (pembrolizumab), терапию против PD-1, одобренную в 2017 году для прогрессирующей карциномы эндометрия, на основе результатов исследования KEYNOTE-158, показывающего значительную эффективность. Такие целенаправленные подходы улучшили результаты по сравнению с традиционной химиотерапией.
Партнерство для объединения Терапия: Признавая необходимость применения многосторонних подходов к лечению, фирмы сотрудничают в целях объединения существующих лекарств. Например, в 2017 году Roche сотрудничала с Flatiron Health, чтобы использовать реальные данные для определения наилучшего использования Tecentriq (atezolizumab) при различных видах рака, включая рак брюшины. Сочетание иммунотерапии, такой как Тецентрик, с химиотерапией, а не только химиотерапией, привело к улучшению показателей ответа. Аналогичным образом, Genentech объединил Tecentriq с химиотерапией в ключевом испытании IMpassion130, что привело к одобрению FDA в 2019 году для лечения метастатического тройного негативного рака молочной железы.
Географическое расширение: Компании расширяют свой портфель лекарств от рака брюшины во всем мире. Например, после получения одобрения США и ЕС для Tecentriq по различным показаниям к раку, включая TNBC, Genentech / Roche теперь подает заявку на одобрение на других ключевых рынках, таких как Китай и Япония, для решения глобальных рыночных возможностей. Это помогает увеличить доходы и обслуживает больше пациентов по всему миру.
Сегментарный анализ Рынок перитонального рака

По типу лекарств продукты поздней стадии составляют существенную долю в прогнозируемом периоде.
По типу лекарств, продукты поздней стадии, как ожидается, внесут наибольшую долю в 70,3% в 2024 году из-за повышения клинической эффективности продуктов поздней стадии, включая препараты, которые прошли клинические испытания и находятся на поздней стадии разработки или уже получили одобрение регулирующих органов, доминируют в сегменте препаратов типа брюшинного рака. Эти препараты продемонстрировали явную клиническую эффективность в лечении рака брюшины посредством обширных клинических исследований. Пациенты и врачи предпочитают использовать методы лечения, которые, как было доказано, безопасно и эффективно нацелены на раковые клетки. Продукты поздней стадии накопили существенные данные клинических испытаний, устанавливая их профили безопасности и эффективности, укрепляя доверие к их способности продлить выживание пациентов и улучшить качество жизни. Производители постоянно работают над расширением клинических показаний и направлений лечения одобренных препаратов на поздних стадиях, что позволяет им лечить более широкие группы пациентов. По мере того, как новые продукты на поздних стадиях получают одобрение, а существующие расширяют свое утвержденное использование, этот сегмент приобретает все большее значение. Его лидерство еще больше усиливается нежеланием врачей широко назначать лекарства, которые еще не доказали свою ценность в поздних испытаниях и нормативных обзорах. Обширные клинические доказательства поздних стадий лечения рака брюшины делают их логичным первым вариантом для пациентов.
По пути управления, устный сегмент, как ожидается, значительно вырастет в прогнозируемый период.
Ожидается, что благодаря преимуществам удобства устный перевод обеспечит самую высокую долю рынка - 45,7%. В сегменте методов лечения рака брюшины наибольшую долю составляют пероральные методы лечения. Ключевым фактором, способствующим доминированию пероральных препаратов, является существенное удобство, которое они предлагают пациентам по сравнению с другими способами введения, такими как внутривенные или подкожные инъекции. Не требуя поездки в клиники или больницы для администрирования, пациентам легче вписать лечение в свою повседневную жизнь. Это улучшает соблюдение графиков дозировки. Пероральные препараты также могут быть самостоятельно введены в домашних условиях. Это дает пациентам более высокую степень независимости и контроля над их лечением. Отсутствие необходимости в инфузионных медицинских процедурах также устраняет определенные риски для здоровья и снижает общую стоимость лечения. Как пациенты, так и врачи предпочитают варианты перорального лечения, когда они являются эффективной альтернативой инъекциям. По мере того, как все больше методов лечения рака брюшины становятся доступными в удобных пероральных лекарственных формах, их простота использования будет продолжать привлекать использование от менее удобных для пациента методов введения.
Дополнительные идеи Рынок перитонального рака
Отчет о перитонеальном раке показывает значительный рост исследований и разработок с более чем 60 препаратами на различных стадиях клинических испытаний. Разработка сосредоточена на новых методах лечения, направленных на улучшение выживаемости пациентов, страдающих этим редким и агрессивным раком. Несмотря на проблемы в ранней диагностике, достижения в области таргетной терапии, такие как ингибиторы PARP и препараты, нацеленные на конкретные киназы, показывают перспективы. В докладе подчеркивается роль циторедуктивной хирургии в сочетании с внутрибрюшинной химиотерапией в качестве ключевого метода лечения, особенно в специализированных центрах. Клинические испытания таких препаратов, как Маситиниб и Азенозертиб, расширяют границы лечения рака брюшины, предлагая новую надежду для пациентов. Активность трубопровода сильна, сотрудничество и слияния стимулируют инновации, которые, как ожидается, положительно повлияют на рынок в ближайшие годы.
Обзор конкурентов Рынок перитонального рака
Основными игроками, работающими на рынке перитонеального рака, являются AB Science, Zentalis Pharmaceuticals, ImmunoGen, Юго-западный медицинский центр UT, Avastin, Roche Holding, Merck & Co Inc, Novartis, GSK, Bayer, AstraZeneca и Synta Pharmaceuticals.
Рынок перитонального рака Лидеры
- AB Наука
- Компания Zentalis Pharmaceuticals
- Иммуноген
- Юго-западный медицинский центр
- Авастин
Рынок перитонального рака - Конкурентное соперничество

Рынок перитонального рака
(Доминируют крупные игроки)
(Высококонкурентный с большим количеством игроков.)
Последние разработки в Рынок перитонального рака
- В мае 2024 года препарат Masitinib от AB Science в клинических испытаниях III фазы нацелен на специфические киназы для ингибирования роста опухоли у пациентов с раком брюшины.
- В апреле 2024 года Zentalis Pharmaceuticals продвигает Azenosertib, ингибитор Wee1, в испытаниях фазы II для нацеливания механизмов восстановления ДНК в раковых клетках, потенциально предлагая новые пути лечения.
- В марте 2024 года выходит IMGN151 от ImmunoGen Фаза Я проводил испытания, демонстрируя многообещающие результаты в нацеливании на опухолевые клетки, экспрессирующие альфа-рецептор фолата (FRα), что дает новую надежду пациентам с низкой экспрессией FRα.
Рынок перитонального рака Сегментация
- Тип препарата
- Продукты поздней стадии
- Продукты среднего уровня
- Продукты ранней стадии
- По маршруту администрации
- устный
- подкожный
- внутривенно

Хотите изучить возможность покупкиотдельные разделы этого отчета?
Часто задаваемые вопросы :
Насколько велик рынок перитонеального рака?
Глобальный рынок перитонеального рака оценивается в 5,9 млрд долларов США в 2024 году и, как ожидается, достигнет 15,9 млрд долларов США. Bn к 2031 году, растущий при совокупных годовых темпах роста (CAGR) 17,9% с 2024 по 2031 год.
Каким будет CAGR рынка перитонеального рака?
Прогнозируется, что CAGR рынка перитонеального рака составит 17,9% с 2024 по 2031 год.
Каковы основные факторы, влияющие на рост рынка перитонеального рака?
Достижения в области целевой терапии, включая ингибиторы PARP и целевые препараты, такие как Авастин, улучшают выживаемость пациентов и варианты лечения, а циторедуктивная хирургия в сочетании с Hipec показала эффективность в контроле симптомов рака брюшины и улучшении результатов лечения пациентов. Это основные факторы, влияющие на рынок перитонеального рака.
Каковы ключевые факторы, препятствующие росту рынка перитонеального рака?
Высокие затраты, связанные с передовыми вариантами лечения, такими как циторедуктивная хирургия и внутрибрюшинная химиотерапия. Проблемы в ранней диагностике из-за неопределенных симптомов, напоминающих другие распространенные состояния, ограничение возможностей лечения являются основным фактором, препятствующим росту рынка перитонеального рака.
Какой тип лекарств является ведущим на рынке перитонеального рака?
Ведущим сегментом лекарственных средств является продукция поздней стадии.
Какие основные игроки работают на рынке перитонеального рака?
AB Science, Zentalis Pharmaceuticals, ImmunoGen, UT Southwestern Medical Center, Avastin, Roche Holding, Merck & Co Inc, Novartis, GSK, Bayer, AstraZeneca, Synta Pharmaceuticals являются основными игроками.