Вирусная вакцина Cell Culture Media Рынок АНАЛИЗ РАЗМЕРОВ И ДОЛЕЙ - ТЕНДЕНЦИИ РОСТА И ПРОГНОЗЫ (2024 - 2031)
Вирусная вакцина Рынок средств массовой информации клеточной культуры сегментируется по типу клеточной культуры (постоянная, приостановка), по типу ср....
Вирусная вакцина Cell Culture Media Рынок Размер
Размер рынка в долларах США Bn
CAGR5.8%
| Период исследования | 2024 - 2031 |
| Базовый год оценки | 2023 |
| CAGR | 5.8% |
| Концентрация рынка | High |
| Основные игроки | Научный Термо Фишер, Мерк, Сарторий, Творческие биолаборатории, Келл и среди других |
дайте нам знать!
Вирусная вакцина Cell Culture Media Рынок Анализ
Рынок медиа-культуры вирусных вакцин оценивается как $1,8 млрд в 2024 году Ожидается, что он достигнет 2,7 млрд долларов к 2031 году, растущие с совокупным годовым темпом роста (CAGR) 5,8% с 2024 по 2031 год. Этот устойчивый рост можно объяснить такими факторами, как увеличение распространенности таких заболеваний, как грипп и COVID-19 во всем мире, а также увеличение инвестиций государственных и частных органов в разработку вакцин.
Ожидается, что на медиарынке вирусных вакцин будет наблюдаться положительный рост в течение прогнозируемого периода. Обеспокоенность по поводу вспышек заболеваний и пандемий стимулировала исследования и разработки вирусных вакцин. Кроме того, развитие методов клеточной культуры для эффективного и крупномасштабного производства вирусных вакцин будет способствовать росту рынка.
Вирусная вакцина Cell Culture Media Рынок Тенденции
Рыночный драйвер - Рост глобального спроса на вирусные вакцины из-за пандемий и новых заболеваний
Постоянно растущая распространенность вирусных инфекций и пандемий во всем мире привела к значительному росту спроса на вирусные вакцины в последнее время. Вспышка пандемии Covid-19, в частности, подчеркнула важность вакцинации для сдерживания распространения и тяжести таких респираторных вирусных заболеваний. Разработка эффективных вакцин требует эффективного производства с помощью клеточных культуральных сред, которые служат средой роста для производства вирусов.
Поскольку производители вакцин стремятся увеличить предложение и расширить доступ для удовлетворения огромного глобального спроса, создаваемого программами вакцинации, потребность в средствах культивирования клеток существенно растет. Создание новых производственных мощностей и дополнительных мощностей ведущими компаниями по производству вакцин способствует дальнейшему росту спроса на средства массовой информации. Кроме того, постоянные усилия по разработке вакцин для новых заболеваний, таких как вирусы Зика, Эбола и Нипах, требуют постоянных инвестиций в исследования, связанные с оптимизацией условий культивирования клеток и лекарственных средств.
В последнее время растущее внимание правительства к иммунизации во всем мире посредством таких инициатив, как ГАВИ и рекомендации по бустерным дозам, также способствовало сильному распространению вирусных вакцин. Растущее пожилое население во всем мире делает их более восприимчивыми к инфекционным заболеваниям и требует новых целей вакцинации. Это хорошо предвещает долгосрочные перспективы как разработки вирусных вакцин, так и производства медиакультуры клеток млекопитающих. В целом, критическая роль, которую играют средства клеточной культуры в крупномасштабном коммерческом производстве всех современных вирусных вакцин посредством надежных и стандартизированных процессов, вероятно, приведет к значительному потреблению в ближайшие годы.
Рыночный драйвер - Переход к сывороточным и животным компонентам
С ростом нормативного давления и переходом промышленности к более чистым методам производства в последние годы широкое признание получили препараты для клеточной культуры без сыворотки и животного происхождения. Традиционное выращивание сывороточных добавок зависит от сырья животного происхождения, такого как сыворотка крупного рогатого скота плода, которая связана с несоответствием партии к партии и риском передачи патогенов. Это требует обширной характеристики и тестирования во время производства.
Напротив, определенные среды с документированным составом обеспечивают более высокую консистенцию и безопасность путем удаления компонентов животного происхождения и сыворотки из процесса в целом. Продвинутые свободные от сыворотки среды, содержащие свободные от белка и химически определенные составы, облегчают надежную репликацию вируса без беспокойства о случайных агентах. Их использование позволяет соблюдать стандарты качества и биосодержания, требуемые регулирующими органами. Кроме того, они повышают эффективность процесса, устраняя ненужные этапы очистки для удаления белков животного происхождения.
Ведущие производители вакцин во всем мире активно инвестируют в понимание поведения клеток в отсутствие сыворотки, чтобы придумать оптимизированные химически определенные и ксено-свободные платформы. Этот сдвиг поддерживает надежное коммерческое производство, обеспечивая при этом биобезопасность. С большим акцентом на аналитические технологии процессов и мониторинг атрибутов материала в режиме реального времени, передовые среды без животных, вероятно, появятся в качестве производственной системы выбора; тем самым ускоряя рост рынка в ближайшие годы.

Вызов рынка - Высокие затраты, связанные с разработкой и производством средств культивирования клеток вирусной вакцины
Разработка и производство средств культивирования вирусных вакцин требует больших капиталовложений и операционных расходов. Производители должны вкладывать значительные средства в шкафы для биобезопасности, биореакторы, оборудование для создания среды и объекты, которые соответствуют строгим стандартам качества и нормативным требованиям. Они также должны использовать высококачественное сырье в процессе создания среды для обеспечения оптимального роста клеток и репликации вируса. Это делает производство СМИ дорогостоящим делом. Кроме того, правила требуют строгого контроля качества на различных этапах производства, что увеличивает производственные затраты. Низкие объемы и специализированный характер средств культивирования клеток вирусной вакцины по сравнению с другими продуктами культивирования клеток также не позволяют экономить на масштабе, что еще больше увеличивает удельные затраты. Высокие затраты представляют собой серьезную проблему для биофармацевтических компаний и могут задержать разработку новых вакцин, особенно для болезней, распространенных в странах с низким и средним уровнем дохода.
Рыночная возможность: расширение сотрудничества и партнерства в области производства вакцин
Ландшафт производства вирусных вакцин свидетельствует о растущем сотрудничестве между исследовательскими институтами, глобальными организациями здравоохранения и производителями. Это помогает объединить ресурсы, а также опыт для более эффективного и доступного производства вакцин. Например, Глобальный альянс по вакцинам и иммунизации (GAVI) поддерживает несколько инициатив по сотрудничеству между производителями из развивающихся и развитых стран в целях передачи технологий и укрепления местного потенциала по производству вакцин. Многие производители также подписывают соглашения о передаче материалов, лицензионные соглашения и контрактные производственные партнерства с новыми организациями по разработке контрактов и производству из Азии и Латинской Америки. Это позволяет использовать их сравнительно недорогую инфраструктуру и квалифицированную рабочую силу. Такие партнерские отношения позволяют более эффективно использовать имеющиеся предприятия по производству вакцин и совместно использовать риски инвестиций. В долгосрочной перспективе они, как ожидается, укрепят глобальные поставки вакцин и снизят затраты за счет эффекта масштаба, что будет способствовать увеличению иммунизации в регионах с низким и средним уровнем дохода.
Предпочтения врачей Вирусная вакцина Cell Culture Media Рынок
Лечение вирусного заболевания обычно следует поэтапному подходу, основанному на стадии инфекции. Для первоначального симптоматического лечения на ранних стадиях, безрецептурные противовирусные препараты, такие как ацетаминофен или ибупрофен, обычно назначаются для снижения лихорадки и болей в организме.
По мере прогрессирования заболевания врачи часто рекомендуют фирменные пероральные противовирусные препараты, такие как Тамифлю (осельтамивир) для пациентов с высоким риском в течение 48 часов после появления симптомов. Для случаев, связанных со вторичными бактериальными инфекциями, могут быть назначены антибиотики, такие как азитромицин (Zithromax). На более тяжелых стадиях применяют внутривенные противовирусные препараты и стероиды. Внутривенные перамивир (Рапиваб) и Дексаметазон (Декадрон) помогают контролировать репликацию вируса и модулировать воспалительный ответ.
Госпитализация рекомендуется для пожилых пациентов или пациентов с существующими заболеваниями легких / сердца, которые повышают риск осложнений. На этих стадиях сильные противовирусные препараты в сочетании с поддерживающей терапией помогают справиться с симптомами и предотвратить повреждение органов. Фавипиравир (Avigan) и Ремдесивир (Veklury) являются двумя новыми противовирусными препаратами широкого спектра действия, набирающими популярность.
Такие факторы, как сопутствующие заболевания, стадия и тяжесть инфекции, профиль риска и наличие новых лекарств в регионе, влияют на решения врачей, назначающих лекарства. Тесный мониторинг пациентов наряду с комбинированной терапией является распространенным явлением на критических стадиях для оптимизации результатов.
Анализ вариантов лечения Вирусная вакцина Cell Culture Media Рынок
Рак легких обычно диагностируется на одной из четырех основных стадий - стадии I до стадии IV - в зависимости от того, как далеко распространился рак. Для ранней стадии рака легких (стадия I-II) хирургия часто является основным вариантом лечения с целью удаления рака из легких. Для пациентов, у которых рак не удаляется хирургическим путем или которые не могут пройти операцию, стереотаксическая лучевая терапия или гипофракционная лучевая терапия предпочтительнее точно доставлять высокие дозы радиации непосредственно в опухоль.
Для более продвинутых видов рака легких (стадия III-IV) обычно рекомендуется химиотерапия. Платиновая двойная химиотерапия с использованием таких препаратов, как цисплатин или карбоплатин в сочетании с другими химиотерапевтическими препаратами, такими как паклитаксел, доцетаксел или пеметрексед, является стандартным лечением первой линии. Для немелкоклеточного рака легких ингибиторы иммунной контрольной точки, такие как пембролизумаб, ниволумаб или атезолизумаб, часто добавляются к химиотерапии на основе экспрессии PD-L1 на опухолевых клетках. Лечение второй линии может включать монотерапию ингибиторами иммунных контрольных точек, ингибиторами ALK/EGFR, такими как алектиниб, кризотиниб или озимертиниб, на основе наличия генетических мутаций. Для отдельных пациентов без мутаций водителя и хорошего состояния производительности используются схемы химиотерапии, такие как доцетаксел или пеметрекс. Эти специализированные мультимодальные методы лечения обеспечивают наилучшие шансы на общий ответ и улучшение выживаемости.
Ключевые выигрышные стратегии, принятые ключевыми игроками Вирусная вакцина Cell Culture Media Рынок
Такие компании, как Thermo Fisher Scientific, значительно инвестировали в НИОКР для разработки новых и более совершенных лекарственных препаратов для клеточной культуры, которые поддерживают высокую вирусную урожайность. В 2018 году Thermo запустила ExpiSfTM Expression Medium, химически определенный носитель для взвешенных клеточных культур. Эти средства массовой информации помогли производителям эффективно увеличить производство вирусных вакцин.
Чтобы расширить свои медиа-предложения по клеточной культуре, многие игроки пошли на приобретения. Например, в 2020 году Merck KGaA приобрела Atlanta Biologicals, лидера в области сывороточных и животных культур клеток. Это укрепило медиапортфель и возможности Merck в производстве вирусных вакцин.
Производители средств массовой информации формируют ключевые партнерские отношения с производителями вакцин для поддержки своих потребностей в НИОКР и коммерческом производстве. Например, в 2015 году «Сарториус» сотрудничал с «Санофи Пастер», поддерживая разработку и производство живой ослабленной вакцины против гриппа с помощью средств культивирования клеток «Сарториус».
Чтобы обеспечить лидерство на быстрорастущем рынке вирусных вакцин, такие игроки, как Thermo Fisher, инвестировали в крупные производственные предприятия. Например, его завод площадью 400 000 кв. футов в Берлингтоне, NC производит сывороточные и химически определенные среды в промышленном масштабе. Эта стратегия обеспечивает адекватное поступление средств массовой информации на рынок.
Медиа-компании также принимают стратегию предложения индивидуальных и специализированных медийных формулировок. Например, средства производства вирусов Irvine Scientific оптимизированы и специально разработаны для конкретных вирусов, таких как вирусные векторы и респираторные вирусы. Этот целевой подход помогает улучшить удержание и удовлетворение клиентов.
Сегментарный анализ Вирусная вакцина Cell Culture Media Рынок
По типу клеточной культуры: легкость прилипания клеток стимулирует рост сегмента культуры клеток
Подсегмент адептов обеспечивает наибольшую долю в 54,7% на рынке средств массовой информации для культивирования вирусных вакцин из-за неотъемлемых преимуществ методов роста адептов. Приличные клеточные линии естественным образом прикрепляются и растут на поверхности культурных сосудов, колб или пластин. Эта легкость прикрепления клеток устраняет необходимость в специализированном оборудовании или методах, необходимых для культивирования клеток суспензии. В результате культивирование клеток более просто и доступно для создания и поддержания в клинических или исследовательских лабораториях.
Простая природа культивирования клеток позволяет получать высокие клеточные урожаи, которые имеют решающее значение для эффективного производства вирусных вакцин. Прилипшие клетки легко размножаются непосредственно на поверхности, обеспечиваемой сосудами культуры. Это облегчает плотные монослои активно растущих и делящихся клеток. Прямой контакт прилипших клеток с поверхностью культуры максимизирует площадь поверхности, доступную для клеточной активности и пролиферации. В результате культивирование клеток-приверженцев является высокопродуктивным и эффективным при генерации огромного количества клеток, необходимых для разработки и производства вирусных вакцин.
Приверженная клеточная культура также хорошо подходит для универсальных методов, используемых в разработке вирусных вакцин. Клетки можно легко наблюдать, вручную пропускать, собирать или обрабатывать при прикреплении к поверхностям. Это позволяет адгезивным клеткам эффективно использоваться в основных исследовательских приложениях, таких как трансфекция, инфекция или анализ с использованием микроскопии. Он также позволяет адаптационным клеткам адаптироваться к крупномасштабным промышленным процессам, таким как суспензия биореактора или культура микроносителей. Гибкость культуры клеток-приверженцев к различным методам и масштабам применения укрепляет ее доминирующее положение на рынке средств массовой информации для культивирования клеток вирусных вакцин.
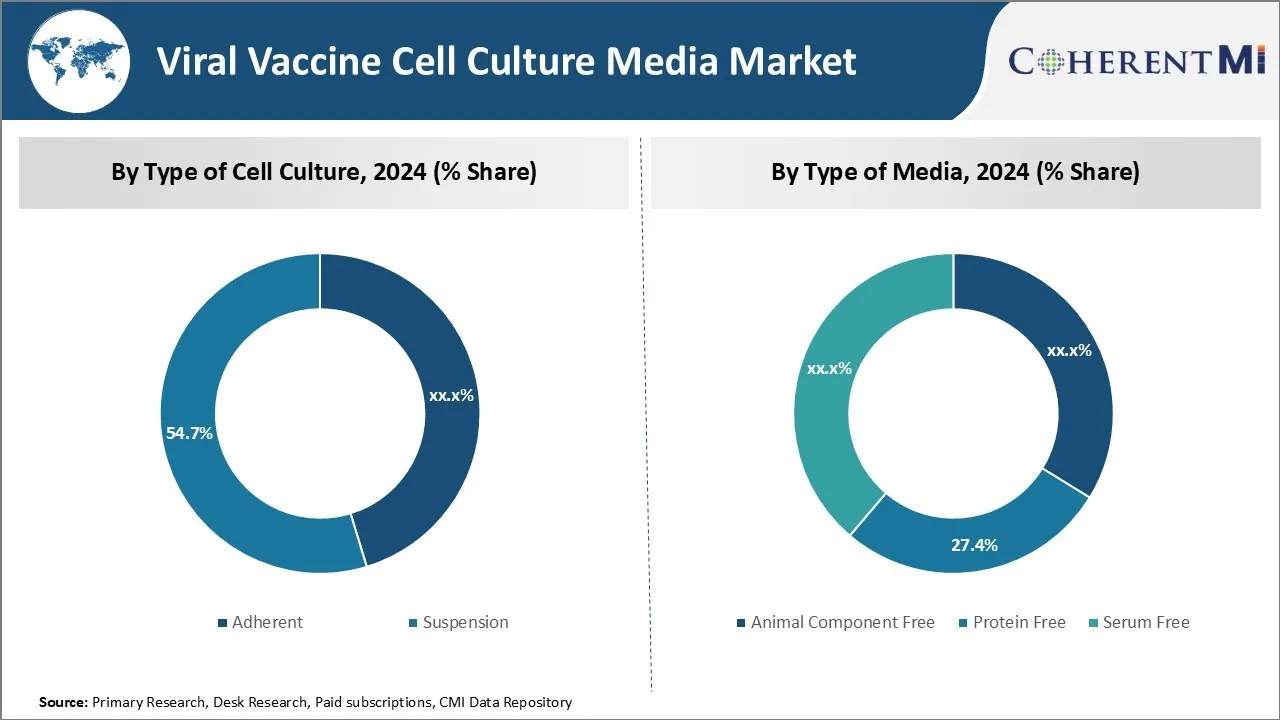
Insights, By Type of Media: Спрос на продукты, не содержащие животных, повышает сегмент медиа без сыворотки
Подсегмент без сыворотки занимает значительную долю в 38,8% на рынке средств массовой информации для культивирования вирусных вакцин из-за повышенного спроса на биопродукцию без животных. Добавки сыворотки, такие как сыворотка крупного рогатого скота плода, содержат нечеловеческие белки и факторы роста, которые могут передавать потенциальные загрязнители в продукты вирусной вакцины человека. Органы регулирования ужесточили требования по удалению компонентов животного происхождения из производственных процессов.
Это привело к тому, что биофармацевтические фирмы приняли свободные от сыворотки средства для производства вирусных вакцин. Препараты без сыворотки точно контролируют клеточные питательные вещества и факторы роста без ненужных животных белков. Эти условия, свободные от животных, обеспечивают определенную воспроизводимую среду, предпочтительную для последовательного производства высококачественных вакцин. Отсутствие сыворотки животных также позволяет избежать потенциальных проблем чистоты, эффективности и безопасности от неизвестных загрязнений.
Спрос также увеличился, поскольку потребители, заботящиеся об этике, ищут вакцины, разработанные без эксплуатации животных. Высокоочищенные средства без сыворотки учитывают эти этические соображения, обеспечивая при этом эффективную культуру клеток и производство вакцин. Ведущие биофармы в настоящее время используют исключительно оптимизированные, свободные от животных среды для удовлетворения нормативных требований и потребительских ценностей в отношении благополучия животных в своих продуктах иммунизации.
Дополнительные идеи Вирусная вакцина Cell Culture Media Рынок
- Ожидается, что мировой рынок средств массовой информации для культивирования вирусных вакцин будет испытывать устойчивый рост, обусловленный повышенным спросом на вакцины в свете недавних пандемий, таких как COVID-19. Рынок характеризуется значительным сдвигом в сторону сывороточных и животных компонентов из-за их более низких показателей загрязнения и более высоких профилей безопасности. Эта тенденция также поддерживается нормативным стремлением к более безопасным и эффективным процессам производства вакцин.
Обзор конкурентов Вирусная вакцина Cell Culture Media Рынок
Основными игроками, работающими на рынке средств массовой информации для культивирования вирусных вакцин, являются Thermo Fisher Scientific, Merck, Sartorius, Creative Biolabs, Xell, Jianshun Biosciences, лаборатории ATZ и OPM Biosciences.
Вирусная вакцина Cell Culture Media Рынок Лидеры
- Научный Термо Фишер
- Мерк
- Сарторий
- Творческие биолаборатории
- Келл
Вирусная вакцина Cell Culture Media Рынок - Конкурентное соперничество

Вирусная вакцина Cell Culture Media Рынок
(Доминируют крупные игроки)
(Высококонкурентный с большим количеством игроков.)
Последние разработки в Вирусная вакцина Cell Culture Media Рынок
- В августе 2023 года BioVaxys Technology расширила свое исследовательское сотрудничество с Университетом штата Огайо, сосредоточившись на исследованиях SARS-CoV-2, SARS-CoV-1 и пансарбековирусной вакцины.
- В марте 2023 года ModeX Therapeutics заключила лицензионное соглашение с Merck о разработке кандидата на вакцину от вируса Эпштейна-Барра (EBV).
- В январе 2023 года Ocugen опубликовала положительные данные для своего кандидата на вакцину от COVID-19 Коваксина в фазе 2/3 испытаний для увеличения иммунобридинга и расширения исследований.
Вирусная вакцина Cell Culture Media Рынок Сегментация
- По типу клеточной культуры
- верный
- Приостановка
- По типу медиа
- Животный компонент бесплатно
- Белок свободный
- Сыворотка свободна

Хотите изучить возможность покупкиотдельные разделы этого отчета?
Часто задаваемые вопросы :
Каковы ключевые факторы, препятствующие росту рынка средств массовой информации для культивирования вирусных вакцин?
Высокие затраты, связанные с разработкой и производством средств культивирования вирусных вакцин и строгие нормативные требования к производству вакцин, являются основными факторами, препятствующими росту рынка средств массовой информации для культивирования вирусных вакцин.
Каковы основные факторы, влияющие на рост рынка медиа-культуры вирусных вакцин?
Растущий глобальный спрос на вирусные вакцины из-за пандемий и новых заболеваний и переход к сывороточным и животным компонентам для снижения рисков загрязнения являются основными факторами, стимулирующими рынок средств массовой информации для культивирования вирусных вакцин.
Что является ведущим типом клеточной культуры на рынке средств массовой информации для вирусных вакцин?
Ведущим типом сегмента клеточной культуры является суспензия.
Какие основные игроки работают на медиа-рынке вирусных вакцин?
Thermo Fisher Scientific, Merck, Sartorius, Creative Biolabs, Xell, Jianshun Biosciences, ATZ labs и OPM Биологические науки являются основными игроками.
Каким будет CAGR на рынке средств массовой информации вирусных вакцинных клеток?
Прогнозируется, что CAGR рынка средств массовой информации для культивирования вирусных вакцин составит 5,8% с 2024 по 31 год.